题目内容
【题目】100 g炭粉燃烧所得气体中,CO占![]() 体积、CO2占
体积、CO2占![]() 体积,且
体积,且
C(s)+![]() O2(g)=CO(g) ΔH=-110.35 kJ·mol-1
O2(g)=CO(g) ΔH=-110.35 kJ·mol-1
CO(g)+![]() O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1
O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-392.92 kJ·mol-1
与这些炭完全燃烧相比较,损失的热量是________。
【答案】784.92 kJ
【解析】
碳不完全燃烧损失的热量为生成的一氧化碳燃烧放出的热量,根据碳原子守恒计算出一氧化碳的物质的量,再根据一氧化碳燃烧的热化学方程式计算。
100g碳的物质的量为![]() =
=![]() mol,则CO的物质的量为
mol,则CO的物质的量为![]() mol×
mol×![]() =
=![]() mol,由于CO(g)+
mol,由于CO(g)+![]() O2(g)=CO2(g)△H=-282.57kJ/mol,所以
O2(g)=CO2(g)△H=-282.57kJ/mol,所以![]() molCO燃烧放出的热量为282.57kJ/mol×
molCO燃烧放出的热量为282.57kJ/mol×![]() mol=784.92kJ,即100g碳不完全燃烧生成
mol=784.92kJ,即100g碳不完全燃烧生成![]() molCO损失的热量为784.92kJ。
molCO损失的热量为784.92kJ。

 名校课堂系列答案
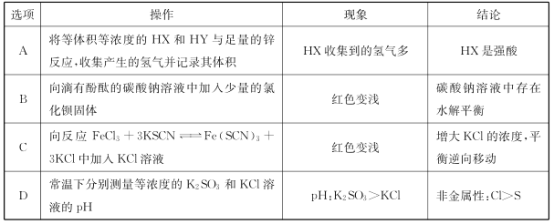
名校课堂系列答案【题目】下列①②对应的试剂(或条件)不能完成实验目的的是( )
![]()
实验目的 | 试剂(条件) | |
A | 温度对Na2S2O3溶液与H2SO4溶液反应速率的影响 | ①热水浴②冷水浴 |
B | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇②煤油 |
C | 用硝酸酸化的AgNO3溶液检验自来水中能否蒸馏除去Cl- | ①自来水②蒸馏水 |
D | 催化剂对H2O2分解速率的影响 | ①0.1mol/LFeCl3 ②0.2mol/LFeCl3 |
A.AB.BC.CD.D
【题目】硫及其化合物有许多用途。相关物质的物理常数如表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____________,基态S原子电子占据最高能级的电子云轮廓图为____________形。
(2)根据价层电子对互斥理论,H2S,SO2,SO3的气态分子中,中心原子价层电子对数不同于其他分子的是____________。
(3)图(a)为S2的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为____________。
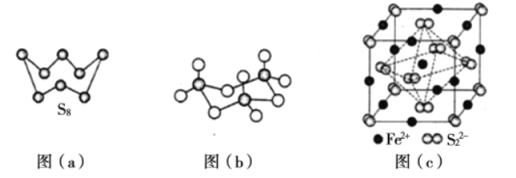
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为____________形,其中共价键的类型有____________种;固体三氧化硫中存在如图(b)所示的三聚分子。该分子中S原子的杂化轨道类型为____________。
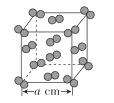
(5) FeS2晶体的晶胞如图(c)所示,晶胞边长为a nm, FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为____________g·cm-3;晶胞中Fe2+位于S22-所形成的八面体的体心,该正八面体的边长为____________nm。