题目内容
【题目】地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题。文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响。
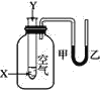
(1)实验前:①先用0.1mol·L-1 H2SO4洗涤Fe粉,其目的是____,然后用蒸馏水洗涤至中性;②将KNO3溶液的pH调至2.5;③为防止空气中的O2对脱氮的影响,应向KNO3溶液中通入____(写化学式)。
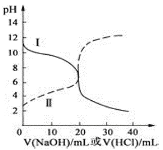
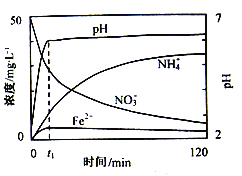
(2)如图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应的离子方程式____。t1时刻后,该反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是____。
(3)该课题组对影响脱氮速率的因素提出了如下假设,请你完成假设二和假设三:
假设一:溶液的pH;
假设二:____;
假设三:____;
(4)请你设计实验验证上述假设一,补充实验步骤及结论:(已知:溶液中的NO3-浓度可用离子色谱仪测定)____、____。

【答案】除去铁粉表面的氧化物等杂质 N2 4Fe+10H++NO3-=4Fe2++NH4++3H2O 生成的Fe2+水解(或和溶液中OH-的结合) 温度 铁粉颗粒大小 pH各不相同,并通入氮气 用离子色谱仪测定相同反应时间时各溶液中NO3-的浓度,若pH不同KNO3溶液中,测出的NO3-浓度不同,表明pH对脱氮速率有影响,否则无影响
【解析】
本题是模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响。
(1)①铁表面的氧化物主要是氧化铁,因此H2SO4可以除去Fe粉表面的氧化物是发生反应的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;故答案为:除去铁粉表面的氧化物等杂质;
②氧气具有氧化性,而空气中含有大量的氧气,所以为防止空气中的O2对脱氮的影响,可向KNO3溶液中通入N2,排出O2;故答案为:N2;
(2)根据图中信息可判断,t1时刻前溶液中离子浓度减小的有:H+、NO3-、增大的有Fe2+、NH4+ ,t1时刻前反应的离子方程式为:4Fe+10H++NO3-=4Fe2++NH4++3H2O ,故
t1时刻后,该反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是发生了水解反应,溶液pH增大,促进水解,故答案为4Fe+10H++NO3-=4Fe2++NH4++3H2O;生成的Fe2+水解(或和溶液中OH-的结合);
(3)影响脱氮速率的因素除了溶液的pH外,还可能是温度、固体与溶液的接触面积等,故答案为:温度;铁粉颗粒大小;
(4)要验证溶液的pH影响脱氮速率,需要设计对照实验,其他条件相同,而pH不同,并通入氮气, 再分别向溶液中分别加入足量等质量的同种铁粉,根据已知用离子色谱仪测定相同反应时间时各溶液中NO3-的浓度,故答案为:pH各不相同,并通入氮气;用离子色谱仪测定相同反应时间时各溶液中NO3-的浓度,若pH不同KNO3溶液中,测出的NO3-浓度不同,表明pH对脱氮速率有影响,否则无影响。

 阅读快车系列答案
阅读快车系列答案