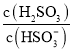题目内容
【题目】下列叙述正确的是( )
A. 将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+)
B. 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C. pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D. 向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中 增大
增大
【答案】C
【解析】
A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,溶液中氢离子浓度等于氢氧根离子浓度;溶液呈电中性,所以阴阳离子所带电量相等,所以2c(SO42-)=c(NH4+),故A错误;
B、醋酸是弱电解质,在水溶液中只有部分电离,所以醋酸的浓度大于氢离子浓度;两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1的两种醋酸溶液中氢离子浓度之比=10:1,当两种酸的电离度相同时,则c1=10c2,实际上,两种酸的浓度不等,且浓度越大,酸的电离度越小,所以两种酸的浓度关系为c1>10c2,故B错误;
C、pH=11的NaOH溶液的c(NaOH)=10-3mol/L,pH=3醋酸溶液的c(CH3COOH)>10-3mol/L,等体积的两种溶液醋酸的物质的量大于氢氧化钠的物质的量,等体积混合后溶液呈酸性,所以向混合液中滴入石蕊试液呈红色,所以C选项是正确的;
D、氨水的电离方程式为:NH3![]() H2ONH4++OH-,当向氨水中加入硫酸铵时,硫酸铵中含有铵根离子,导致氨水的电离平衡向逆反应方向移动,溶液中氢氧根离子浓度降低,氨水的浓度增大,则溶液中
H2ONH4++OH-,当向氨水中加入硫酸铵时,硫酸铵中含有铵根离子,导致氨水的电离平衡向逆反应方向移动,溶液中氢氧根离子浓度降低,氨水的浓度增大,则溶液中![]() 减小,故D错误。
减小,故D错误。
答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在某一容积为5 L的密闭容器中,进行如下化学反应: CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
T /℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =______________。
(2)该反应为____________反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是________________。
a 容器中压强不变 b 混合气体中 c(CO)不变
c υ正(H2)=υ逆(H2O) d c (CO2)=c (CO)
(4)830℃下,若物质的浓度关系是c (CO2)·c (H2) > c (CO)·c (H2O),则此时正反应速率与逆反应速率的关系是____________。
a υ正 > υ逆 b υ正 = υ逆 c υ正 < υ逆 d 无法判断
(5)若开始时向该容器中加入CO2和H2各0.1 mol,在830℃和催化剂存在的条件下,反应达到平衡时,水蒸气的物质的量浓度c(H2O)=_______________。
【题目】由碳酸锰矿(主要成分MnCO3,还含有FeCO3、MnO2、Al2O3、SiO2等)中提取金属锰的一种流程如下:

(1) “酸浸”过程中,提高锰元素浸出率的措施有:适当提高酸的浓度、________________(填一种)。
(2) 保持其他条件不变,在不同温度下对碳酸锰矿进行酸浸,锰元素的浸出率随时间变化如下图所示,则酸浸的最佳温度和时间分别是________。

提取过程中相关金属离子生成氢氧化物沉淀的pH
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀的pH | 1.8 | 5.8 | 3.0 | 7.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.8 |
(3) 已知“酸浸”后溶液中锰元素只以Mn2+形式存在,则“酸浸”中发生氧化还原反应的离子方程式为________________________________________。
(4) 结合上表,“除铁、铝”时加入氨水控制反应液pH的范围为________。
(5) 若上述流程中加入的H2O2不足量,则待电解溶液中会有铁元素残余,进而会影响最终锰的纯度。请设计简要实验方案加以验证待电解溶液中是否含有铁元素: _________________。
(6) 以石墨为电极电解除铁、铝后的溶液获得单质锰。电解废液中可循环利用的溶质是________。