题目内容
15.在一个不导热的密闭反应器中.只发生下列两个反应:a(g)+b(g)?2c(g) AH2<0;x(g)+3y(g)?2z(g)△H2>0进行相关搡作且达到平衡后(忽略体积改变所做的功).下列叙述错误的是( )| A. | 等压时,通入惰性气体,c的物质的量不变 | |
| B. | 等压时,通入z气体反应器中温度升高 | |
| C. | 等容时,通入惰性气体,各反应速率不变 | |
| D. | 等容时,通入z气体,通入z气体的转化率较小 |
分析 A、等压时,通入惰性气体,体积增大,对第二个反应平衡向逆反应移动,温度升高,导致第一个反应向逆反应移动;
B、等压时,通入z气体,第二反应平衡向逆反应移动,反应器中温度升高;
C、等容时,通入惰性气体,各反应混合物的浓度不变;
D、等容时,通入z气体,第二反应平衡向逆反应移动.
解答 解:A、等压时,通入惰性气体,容器体积增大,等效为压强减小,平衡x(g)+3y(g)?2z(g)(△H>0)向左移动,正反应为吸热反应,反应体系的温度降低,由于该反应容器是一个不导热的容器,所以平衡a(g)+b(g)?2c(g)也向由(吸热方向)移动,c的物质的量增大,故A错误;
B、等压时,通入z气体,增大了生成物的浓度,平衡x(g)+3y(g)?2z(g)向左移动,由于该反应的逆反应是放热反应,容器内温度升高,虽然导致第一个反应向逆反应移动,但移动结果不会恢复到原温度,故平衡时温度升高,故B正确;
C、等容时,通入惰性气体,各反应物和生成物的物质的量没有变化,即各组分的浓度没有发生变化,所以各组分的反应速率不发生变化,故C正确;
D、等容时,通入z气体,增大了生成物z的浓度,虽然平衡逆向移动,但气体z的转化率仍然较小,故D正确;
故选A.
点评 本题考查外界条件对化学平衡的影响,难度中等,本题要特别注意题干中的信息“不导热的密闭反应器”,注意压强对第一个反应没有影响,根据第二反应的移动热效应,判断第一个反应的移动.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.对于100mL1mol/L盐酸与铁片的反应,采取下列措施:①升高温度;②改用100mL3mol/L盐酸;③多用300mL1mol/L盐酸;④用等量铁粉代替铁片;⑤改用98%的硫酸;其中能使反应速率加快的是( )
| A. | ①④⑤ | B. | ①②④ | C. | ②③④ | D. | ②③⑤ |
10.下列说法正确的是( )
| A. | 放热反应一定能自发的进行 | |
| B. | SO2能使品红溶液和溴水褪色,说明SO2具有漂白性 | |
| C. | 将AlCl3溶液和Al2(SO4)3溶液分别蒸干灼烧,所得产物的成分均为Al2O3 | |
| D. | 由反应AgCl(s)+KI(aq)?AgI(s)+KCl(aq)可知Ksp(AgCl)>Ksp(AgI) |
5.将足量SO2气体通入下列各组溶液中,所含离子还能大量共存的是( )
| A. | Ba2+、Ca2+、Br-、Cl- | B. | CO32-、SO32-、K+、NH4+ | ||
| C. | Na+、NH4+、I-、HS- | D. | Na+、Ca2+、ClO-、NO3- |
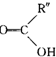
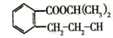 在酸性条件下水解生成M和N:
在酸性条件下水解生成M和N: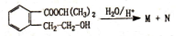
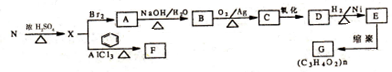
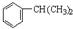 .
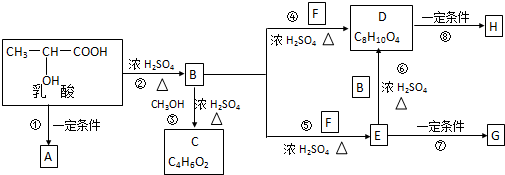
.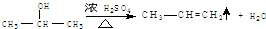 ,E转化为G的化学方程式为
,E转化为G的化学方程式为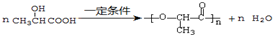 .
.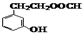 .
.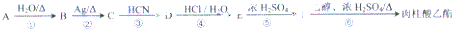
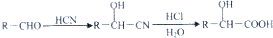
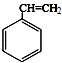 ,肉酸乙酯的结构简式
,肉酸乙酯的结构简式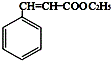 .
.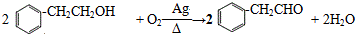 .
.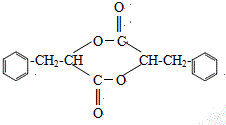 ;H是另一种副产物,它 是一种高分子化合物,形成这种物质的反应类型为缩聚反应.
;H是另一种副产物,它 是一种高分子化合物,形成这种物质的反应类型为缩聚反应.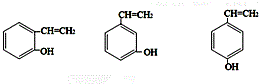 (填结构简式).
(填结构简式).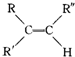 $→_{H_{2}SO_{4}}^{KMnO_{4}}$
$→_{H_{2}SO_{4}}^{KMnO_{4}}$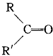 +
+
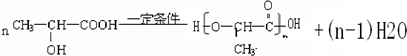 .
.