题目内容
7.已知A~G中均含有羧基,且有以下转化关系.根据转化关系回答下列各题:
根据以上信息回答下列问题:
(1)A的相对分子质量为166.
(2)化合物G的结构简式为
 ;
;(3)实现A-E转化的反应类型是取代反应;实现E-F转化的一定条件是氢氧化钠醇溶液、加热;
(4)化合物B在Ni催化条件能与H2发生加成,理论上1mol B最多可能消耗H2的物质的量为4mol;
(5)写出B与银氨溶液反应的方程式:
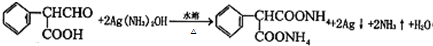 .
.
分析 有机物A、B、C、D、E、F、G均含有羧基,结合各物质分子式可知均含有1个苯环,B能与银氨溶液反应,则B中还含有-CHO,A发生信息①的氧化反应生成B,可推知A中还含有醇羟基,且该醇羟基能氧化成醛基,由D结构可知A中只有一个侧链,故A为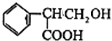 ,B为
,B为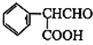 ,C为
,C为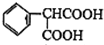 ,E为
,E为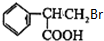 ,由E与F的分子式可知,E在氢氧化钠醇溶液、加热条件下发生消去反应生成F,则F为
,由E与F的分子式可知,E在氢氧化钠醇溶液、加热条件下发生消去反应生成F,则F为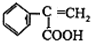 ,F发生加聚反应生成高聚物G为
,F发生加聚反应生成高聚物G为 ,据此解答.
,据此解答.
解答 解:有机物A、B、C、D、E、F、G均含有羧基,结合各物质分子式可知均含有1个苯环,B能与银氨溶液反应,则B中还含有-CHO,A发生信息①的氧化反应生成B,可推知A中还含有醇羟基,且该醇羟基能氧化成醛基,由D结构可知A中只有一个侧链,故A为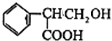 ,B为
,B为 ,C为
,C为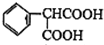 ,E为
,E为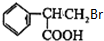 ,由E与F的分子式可知,E在氢氧化钠醇溶液、加热条件下发生消去反应生成F,则F为
,由E与F的分子式可知,E在氢氧化钠醇溶液、加热条件下发生消去反应生成F,则F为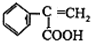 ,F发生加聚反应生成高聚物G为
,F发生加聚反应生成高聚物G为 ,
,
(1)A为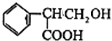 ,A的相对分子质量为166,
,A的相对分子质量为166,
故答案为:166;
(2)化合物G的结构简式为 ,
,
故答案为: ;
;
(3)A-E转化的反应类型是:取代反应,实现E→F转化的一定条件是:氢氧化钠醇溶液、加热,
故答案为:取代反应;氢氧化钠醇溶液、加热;
(4)化合物 在Ni催化条件能与H2发生加成,苯环与醛基都能发生加成反应,理论上1mol
在Ni催化条件能与H2发生加成,苯环与醛基都能发生加成反应,理论上1mol  最多可能消耗H2的物质的量为4mol,
最多可能消耗H2的物质的量为4mol,
故答案为:4mol;
(5)B与银氨溶液反应的方程式为: ,
,
故答案为: .
.
点评 本题考查有机物推断,注意根据有机物的分子式及反应条件进行推断,侧重考查学生分析推理能力,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
相关题目
3.100℃时,若将0.100mol N2O4气体放入1L密闭容器中,发生反应N2O4?2NO2,c(N2O4)随时间的变化如表所示.回答下列问题:
(1)在0~40s时段,化学反应速率v(NO2)为0.0025mol•L-1•s-1;
此温度下的化学平衡常数K为0.36.
(2)下列能说明该反应达到平衡状态的是BD
A.2v(N2O4)=v(NO2)
B.体系的颜色不再改变
C.混合气体的密度不再改变
D.混合气体的压强不再改变
(3)该反应达到平衡后,降温至50℃,c(N2O4)变为0.080mol•L-1,混合气体的颜色变浅(填“深”或“浅”),该反应的正反应为吸热反应(填“吸热”或“放热”),判断的理由是降低温度平衡向放热反应方向移动,降低温度c(N2O4)浓度增大,平衡逆向移动.
(4)该反应达平衡后,若只改变一个条件,达新平衡时,下列能使NO2的体积分数增大的是:BC
A.充入一定量的NO2
B.增大容器的容积
C.分离出一定量的NO2
D.充入一定量的N2
(5)100℃时,若将9.2gNO2和N2O4气体放入1L密闭容器中,某时刻测得容器内气体的平均相对分子质量为50,则此时v正(N2O4)<v逆(N2O4).(填“>”、“=”或“<”)
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol•L-1) | 0.100 | 0.070 | 0.050 | 0.040 | 0.040 | 0.040 |
此温度下的化学平衡常数K为0.36.
(2)下列能说明该反应达到平衡状态的是BD
A.2v(N2O4)=v(NO2)
B.体系的颜色不再改变
C.混合气体的密度不再改变
D.混合气体的压强不再改变
(3)该反应达到平衡后,降温至50℃,c(N2O4)变为0.080mol•L-1,混合气体的颜色变浅(填“深”或“浅”),该反应的正反应为吸热反应(填“吸热”或“放热”),判断的理由是降低温度平衡向放热反应方向移动,降低温度c(N2O4)浓度增大,平衡逆向移动.
(4)该反应达平衡后,若只改变一个条件,达新平衡时,下列能使NO2的体积分数增大的是:BC
A.充入一定量的NO2
B.增大容器的容积
C.分离出一定量的NO2
D.充入一定量的N2
(5)100℃时,若将9.2gNO2和N2O4气体放入1L密闭容器中,某时刻测得容器内气体的平均相对分子质量为50,则此时v正(N2O4)<v逆(N2O4).(填“>”、“=”或“<”)
4.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | Cu溶于稀硝酸HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| C. | Fe2(SO4)3溶液和Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
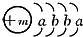 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.



 .
.