题目内容
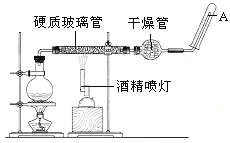
【题目】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验:
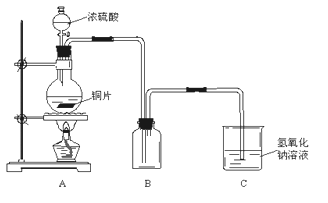
(1)实验中他们取6.4g铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜跟浓硫酸反应的化学方程式:___________________________________________
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是:____________________。
③下列药品中能够用证明反应结束后的烧瓶中确有余酸的是:________(填写字母编号)。
A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(2)为定量测定余酸的物质的量浓度,某位同学进行了如下设计:先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度。他认为测定SO2的量的方法有多种,请问下列实验方案中可行的是__________(填写字母编号)。其中计算结果余酸物质的量浓度比实际偏高的是_______________(填写字母编号)
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀(已知:硝酸具有强氧化性)
若A项不可行,请写出改进的方法:___________________(若A项可行则该空写“不用改进”)
【答案】 ①Cu + 2H2SO4(浓)![]() CuSO4+ SO2↑+ 2H2O 随着反应进行,硫酸被消耗,且产物有水生成,所以浓硫酸变成稀硫酸,反应会停止 AD E C A产生的气体先经浓硫酸干燥,后用碱石灰吸收
CuSO4+ SO2↑+ 2H2O 随着反应进行,硫酸被消耗,且产物有水生成,所以浓硫酸变成稀硫酸,反应会停止 AD E C A产生的气体先经浓硫酸干燥,后用碱石灰吸收
【解析】(1)①铜跟浓硫酸加热反应生成硫酸铜和二氧化硫等;正确答案:Cu + 2H2SO4(浓)![]() CuSO4+ SO2↑+ 2H2O;
CuSO4+ SO2↑+ 2H2O;
②随着反应进行,硫酸被消耗,且产物有水生成,所以浓硫酸变成稀硫酸,铜与稀硫酸不反应,反应会停止;正确答案:随着反应进行,硫酸被消耗,且产物有水生成,所以浓硫酸变成稀硫酸,反应会停止;
③金属铁与稀硫酸反应产生气体,A正确;溶液中有硫酸铜和稀硫酸,硫酸根离子都能与钡离子反应生成硫酸钡沉淀,无法证明结论;B错误;银与稀硫酸不反应,没有现象,无法证明;C错误;碳酸氢钠溶液与稀硫酸反应生成二氧化碳气体,D正确;正确选项:AD;
(2)SO2中混有水蒸气,碱石灰也吸收水蒸气,SO2的量偏大,测定余酸物质的量浓度偏小;A错误;
SO2能够被稀硫酸酸化的高锰酸钾溶液氧化为硫酸根离子,与氯化钡溶液反应生成沉淀,稀硫酸中还有硫酸根离子,SO2的量偏大,根据硫原子守恒规律,所测余酸物质的量浓度偏小;B错误;
SO2以1:40溶解于水,且和水发生反应,SO2的量偏小,根据硫原子守恒规律,所测余酸物质的量浓度偏大,C错误;
SO2气体与氢氧化钡溶液反应,生成亚硫酸钡沉淀,该沉淀在空气中易被氧化为硫酸钙,导致固体质量增加,SO2的量偏大,根据硫原子守恒规律,测定余酸物质的量浓度偏小; D错误;
SO2被硝酸氧化为硫酸根离子,然后再与钡离子结合生成硫酸钡沉淀,反应完全后,过滤、洗涤、干燥、称量沉淀,结果准确;E正确;
正确选项:E;C;
A项中主要是水蒸气被碱石灰吸收带来的误差,导致所测SO2的含量增大,所以要除去水蒸气,用浓硫酸即可;正确答案:A产生的气体先经浓硫酸干燥,后用碱石灰吸收;

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案