题目内容
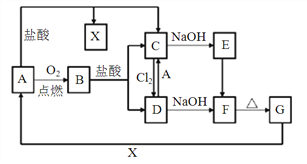
【题目】有关物质转化关系如下图,已知A是一种常见金属,F是一种红褐色沉淀。回答下列问题。
(1)A的化学式为_______;
(2)实验室保存C溶液时需加少量固体A,目的是_____________________。B与盐酸反应的离子方程式为_____________________________。
(3)检验C溶液中阳离子常用的方法是______________________________。
(4)E的浊液在空气中会变质生成F,对应现象为_______________________________ 。
(5)向C中加入Na2O2也可实现C向D和F的转化,Na2O2完全被还原。反应的离子方程式为________________________________。
【答案】 Fe 防止Fe2+被氧化 Fe3O4+8H+Fe2++2Fe3++4H2O 取少量溶液于试管中,滴加KSCN溶液,无明显现象,再滴加氯水,溶液出现血红色 白色沉淀迅速转化为灰绿色,最后形成红褐色的沉淀。 3Na2O2+6H2O+6Fe2+=4Fe(OH)3+6Na++2Fe3+
【解析】A是一种常见金属,F是一种红褐色沉淀,由转化关系可知F为Fe(OH)3,A为Fe,Fe与氧气反应生成的B为Fe3O4,四氧化三铁与盐酸反应得到氯化亚铁与氯化铁,故Fe与盐酸反应得到X为氢气、C为FeCl2,可推知E为Fe(OH)2、D为FeCl3,G为Fe2O3。
(1)A的化学式为Fe;FeCl2易被空气中氧气氧化,保存FeCl2溶液时加固体Fe,防止Fe2+被氧气氧化;B与盐酸反应的离子方程式为:Fe3O4+8H+ =Fe2++2Fe3++4H2O;(3)D为FeCl2,含有阳离子为Fe2+,检验Fe2+离子的方法为:取少量溶液于试管中,滴加KSCN溶液,无明显现象,再滴加氯水,溶液出现血红色 ;(4)E转化为F是氢氧化亚铁被氧气氧化生成氢氧化铁,反应现象为:白色沉淀迅速转化为灰绿色,最后形成红褐色的沉淀。(5)向FeCl2中加入Na2O2也可实现FeCl2向FeCl3和Fe(OH)3的转化,Na2O2完全被还原。反应的离子方程式为:3Na2O2+6H2O+6Fe2+=4Fe(OH)3+6Na++2Fe3+。