题目内容
根据你学习的有关氨的知识,完成下面的问题。
(1)合成氨对化学工业具有重要意义。写出氨的两种重要用途_________;__________。
(2)实验室制备氨气,下列方法中最适宜选用的是______________。
①固态氯化氨加热分解
②固体氢氧化钠中滴加浓氨水
③氯化氨溶液与氢氧化钠溶液共热
④固态氯化氨与氢氧化钙混和加热
(1)合成氨对化学工业具有重要意义。写出氨的两种重要用途_________;__________。
(2)实验室制备氨气,下列方法中最适宜选用的是______________。
①固态氯化氨加热分解
②固体氢氧化钠中滴加浓氨水
③氯化氨溶液与氢氧化钠溶液共热
④固态氯化氨与氢氧化钙混和加热
(1)制化肥 制硝酸(液氨作制冷剂) (2)②④
试题分析:(1)氨气是中学中唯一的碱性气体,重要的用途是制造化肥、合成硝酸以及作为制冷剂等;
(2)氯化氢分解生成氨气和氯化氢,气体冷却后又生成氯化铵,①不正确;氢氧化钠溶于水放出大量的热量,且增大溶液中OH-浓度,进一步促进氨水分解生成氨气,②正确;氯化氨溶液与氢氧化钠溶液共热,生成的氨水浓度太小,得不到氨气,③不正确;④是实验室制取氨气的,正确,答案选②④。
点评:该题难度不大,属于基础性试题。氨气的用途需要熟练记住。关于氨气的制备除了掌握实验室制取的原理以外,还可以利用氨水的不稳定性,通过分解生成。

练习册系列答案
相关题目
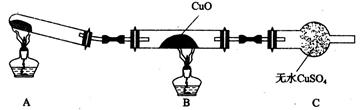
 CuO
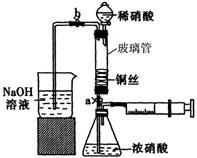
CuO 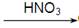 Cu(NO3)2
Cu(NO3)2 CuO
CuO 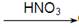 Cu(NO3)2
Cu(NO3)2