题目内容
【题目】在人类社会的发展进程中,金属起着重要的作用。
(1)以下有关金属单质的叙述正确的是_______。
A.金属钠非常活泼,在实验室中保存在石蜡油或煤油中
B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,并有熔融物滴下
C.铁单质与水蒸气反应的化学方程式为2Fe+3H2O(g)=Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如下图所示,试回答:
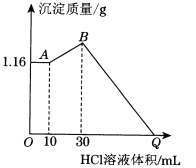
①A点的沉淀物的化学式为________;B点的沉淀物的化学式为________________________;写出A→B段发生反应的离子方程式_____________________________。
②原混合物中MgCl2的质量是________g,AlCl3的质量是________g,NaOH的质量是________g。
③Q点HCl溶液加入量是________mL。
【答案】A Mg(OH)2 Mg(OH)2和Al(OH)3 AlO2-+H++H2O=Al(OH)3↓ 1.90 2.67 5.20 130
【解析】
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的浊液中逐滴加入1 mol·L-1 HCl溶液,前10毫升盐酸反应时沉淀量不变,说明盐酸和氢氧化钠反应,则白色沉淀为氢氧化镁沉淀,再加入盐酸产生沉淀,是偏铝酸钠和盐酸反应生成氢氧化铝沉淀,再加入盐酸,氢氧化镁和氢氧化铝沉淀全部溶解。据此解答。
(1) A.金属钠非常活泼,容易和水或氧气反应,在实验室中保存在石蜡油或煤油中,故正确;B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,外面有氧化铝薄膜包着,不会滴下,故错误;C.铁单质与水蒸气反应的化学方程式为2Fe+4H2O(g)![]() Fe3O4+4H2,故错误。故选A;
Fe3O4+4H2,故错误。故选A;
(2) ①先加入的盐酸和氢氧化钠反应,说明白色沉淀为 Mg(OH)2,再加入盐酸,又产生了氢氧化铝沉淀,所以B点为 Mg(OH)2和Al(OH)3 ;A到B的离子方程式为:AlO2-+H++H2O=Al(OH)3↓;
②氢氧化镁沉淀的质量为1.16克,即0.02mol氢氧化镁,则对应的氯化镁的物质的量为0.02mol,质量为0.02mol×95g/mol= 1.90g, 根据AlO2-+H++H2O=Al(OH)3↓分析,反应消耗的盐酸的物质的量为1mol/L×(30-10)×10-3L=0.02mol,则氯化铝的物质的量为0.002mol质量为0.02mol×133.5g/mol= 2.67g,氢氧化钠的物质的量为0.02×2+0.02×4+1×0.01=0.13mol,则质量为0.13 mol ×40 g/mol = 5.20g;
③Q点HCl溶液可以看成就是将原来的氢氧化钠反应生成氯化钠,故根据0.13mol氢氧化钠计算,盐酸的物质的量为0.13mol,体积为![]() =130mL。
=130mL。

 阅读快车系列答案
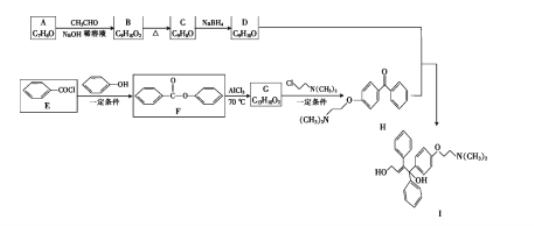
阅读快车系列答案【题目】根据下面的合成路线图完成下面小题

【1】化合物D的名称为( )
A.乙醇B.乙烷C.葡萄糖D.乙酸
【2】乳酸的一种合成方法如图所示,下列说法正确的是( )
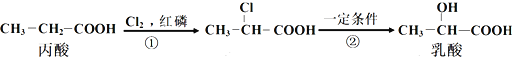
A.步骤①、②分别是加成反应、取代反应
B.蛋白质水解也可生成乳酸
C.丙酸烃基上的二氯代物有2种
D.乳酸与丙烯完全燃烧的产物相同
【3】有下列三种有机物,实现它们之间相互转化所选试剂(均足量)正确的是____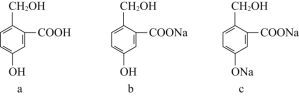
a转化为b | a转化为c | c转化为b | |
A | NaOH | Na | CO2 |
B | Na2CO3 | NaOH | HCl |
C | NaHCO3 | NaOH | CO2 |
D | NaHCO3 | Na2CO3 | HCl |
A.AB.BC.CD.D
【4】化合物A(C4H8Br2)可由下列反应制得,C4H10O![]() C4H8
C4H8![]() C4H8Br2,则A的结构式不可能的是( )
C4H8Br2,则A的结构式不可能的是( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()