题目内容
【题目】已知下列转化关系图,且知采用电解熔融氯化钠的方法可以生产金属钠:2NaCl(熔融)![]() 2Na+Cl2↑,下列说法不正确的是( )
2Na+Cl2↑,下列说法不正确的是( )

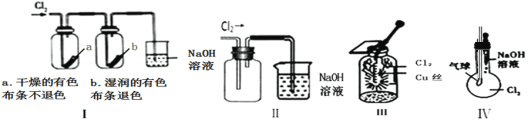
A.A、C、E一定含有同种元素B.若在B中点燃铜丝会产生棕黄色烟
C.C与D反应会产生红褐色沉淀D.D物质可能为FeCl2
【答案】D
【解析】
电解熔融的氯化钠生成Na和Cl2,其中A能与水反应生成C,B能与Fe反应生成D,则A为Na、B为Cl2、D为FeCl3;A与水反应生成的C能与FeCl3反应生成NaCl,C为NaOH;CO2与NaOH反应生成E,FeCl3与Ca(OH)2反应生成F,E与F反应生成NaCl,则E为Na2CO3、F为CaCl2;据此分析作答。
电解熔融的氯化钠生成Na和Cl2,其中A能与水反应生成C,B能与Fe反应![]() 生成D,则A为Na、B为Cl2、D为FeCl3;A与水反应生成的C能与FeCl3反应生成NaCl,C为NaOH;CO2与NaOH反应生成E,FeCl3与Ca(OH)2反应生成F,E与F反应生成NaCl,则E为Na2CO3、F为CaCl2;
生成D,则A为Na、B为Cl2、D为FeCl3;A与水反应生成的C能与FeCl3反应生成NaCl,C为NaOH;CO2与NaOH反应生成E,FeCl3与Ca(OH)2反应生成F,E与F反应生成NaCl,则E为Na2CO3、F为CaCl2;
A.根据上述分析,A、C、E中都含有Na元素,A正确;
B.B为Cl2,铜丝在Cl2中燃烧产生棕黄色的烟,B正确;
C.C为NaOH,D为FeCl3,C与D反应的化学方程式为3NaOH+FeCl3=Fe(OH)3↓+3NaCl,产生红褐色Fe(OH)3沉淀,C正确;
D.由于Cl2具有强氧化性,Fe与Cl2反应生成的D为FeCl3,D错误;
答案选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目