题目内容
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.39g苯分子中含有的碳碳双键数为1.5NA |
| B.1molCH3COONa和少量CH3COOH溶于水所得中性溶液中,CH3COO-数目为NA |
| C.2.24LNH3中含共价键数目一定为0.3NA |
| D.5.6gFe投入100mL 3.5mol·L-1稀硝酸中,充分反应,转移电子总数为0.3 NA |
B
解析试题分析:A、苯分子中不存在单双键交替的结构,错误;B、醋酸钠和醋酸混合溶液中,电荷守恒式为n(Na+)+n(H+)=n(CH3COO-)+n(OH-),因溶液呈中性,所以n(Na+)=n(CH3COO-)=1mol,正确; C、缺少标准状况,错误;D、当Fe与HNO3物质的量比为1:4时,生成硝酸铁。当Fe与HNO3物质的量比为3:8时,生成硝酸亚铁。题中Fe与HNO3物质的量比为1:3.5,所以生成硝酸铁与硝酸亚铁的混合物,错误。
考点:阿伏伽德罗常数

练习册系列答案
相关题目
若NA表示阿伏加德罗常数,下列说法正确的是
| A.Na2O和Na2O2的混合物共1mol,阴离子数目在NA~2NA之间 |
| B.常温常压下,92 g NO2和N2O4的混合气体中含有的分子数目为2NA |
| C.一定条件下,密闭容器充入1molN2和3molH2充分反应,转移电子的数目为6NA |
| D.FeCl3溶液中,若Fe3+数目为NA,则Cl—数目大于3NA |
称取两份铝粉,第一份中加入足量的盐酸,第二份中加入足量的烧碱,若同温同压下放出相同体积的气体,则两份铝粉的质量比为
| A.2∶3 | B.1∶6 | C.3∶2 | D.1∶1 |
一定量的锌与100mL18.5mol?L﹣1的浓H2SO4充分反应后,锌完全溶解,同时生成标准状况下的气体33.6L.将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1mol?L﹣1.则生成的气体中SO2和H2的体积比为( )
| A.1:2 | B.2:1 | C.1:4 | D.4:1 |
NA为阿伏伽德罗常数,下列叙述错误的是( )
| A.1mol乙醇中含有C—H键的数目为6 NA |
| B.46gNO2和N2O4混合气体中含有原子总数为3NA |
| C.足量Na 与1 mol O2反应,,转移电子可能为4NA个 |
D.常温下,1L 0.1 0mol.L-1的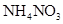 溶液中氮原子数为0.2 溶液中氮原子数为0.2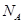 |
NA代表阿伏加德罗常数。下列叙述正确的是
| A.标准状况下,22.4L己烷中C-C共价键数目为5NA |
| B.0.1mol·L¯1AlCl3溶液中含有氯离子数为0.3NA |
| C.1molFe在1molCl2中充分燃烧,转移电子数为3NA |
| D.20g重水(2 1H2O)所含的电子数为10NA |
用NA表示阿伏加德罗常数,下列叙述正确的是(相对原子质量:N—14 H—1)
| A.1L0.1mol?L―lNaHCO3溶液中含有0.1NA个HCO3― |
| B.17g氨气中含有的氢原子数为3NA |
| C.标准状况下,2.24LC2H4中含共价键数为0.4NA |
| D.常温常压下,2.24L甲烷中含有甲烷分子数为0.1NA |
将一定量的NaOH和NaHCO3的混合物X放在密闭容器中加热,充分反应后生成V1L气体Z(V1≠0)。反应后的固体残渣Y与过量的稀盐酸反应,又生成V2L气体Z(V1、V2均为标准状况下气体的体积)。下列判断不正确的是
| A.V1>V2 | B.Z的成分为CO2 |
| C.Y的成分为 Na2CO3 | D.X中 mol mol |
设NA为阿伏加德罗常数的值,下列判断正确的是
| A.1 mol·L-1 FeCl3溶液,含有Fe3+的数目为NA个 |
| B.标准状况下,22.4L辛烷中分子数目为NA个 |
| C.0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3 NA个 |
| D.氧气和臭氧组成的4.8g混合气体中含有0.3 NA个氧原子 |