题目内容
若NA表示阿伏加德罗常数,下列说法正确的是
| A.Na2O和Na2O2的混合物共1mol,阴离子数目在NA~2NA之间 |
| B.常温常压下,92 g NO2和N2O4的混合气体中含有的分子数目为2NA |
| C.一定条件下,密闭容器充入1molN2和3molH2充分反应,转移电子的数目为6NA |
| D.FeCl3溶液中,若Fe3+数目为NA,则Cl—数目大于3NA |
D
解析试题分析:A.Na2O和Na2O2的混合物共1mol,阴离子数目NA。过氧化钠中含有的阴离子为过氧根离子;B.因为2NO2 N2O4,常温常压下,92 g NO2和N2O4的混合气体中含有的分子数目小于2NA;C.工业合成氨是个可逆反应,不能彻底完成,一定条件下,密闭容器充入1molN2和3molH2充分反应,转移电子的数目小于6NA。
N2O4,常温常压下,92 g NO2和N2O4的混合气体中含有的分子数目小于2NA;C.工业合成氨是个可逆反应,不能彻底完成,一定条件下,密闭容器充入1molN2和3molH2充分反应,转移电子的数目小于6NA。
考点:考查阿伏伽德罗常数及相关计算,属于高考必考考点,复习时要加强练习。

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.1mol SiO2中含有NA个SiO2分子 |
| B.1mol Cu与足量的稀HNO3反应,转移2 NA个电子 |
| C.1 L0.1mol . L-1Na2CO3溶液中含有 0.1NA个CO32- |
| D.1mol苯乙烯中含有的碳碳双键数为4NA |
下列化学用语不正确的是
A.二氧化碳的电子式是: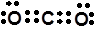 |
B.铝离子的结构示意图是: 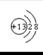 |
C. 的中子数与质子数之差是2 的中子数与质子数之差是2 |
| D.Na2O2中的阳离子数与阴离子数之比为1:1 |
向mg铁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。
随即向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使与硫酸反应所得的金属离子刚
好沉淀完全,并在空气中放置较长时间至沉淀不再发生改变,得到沉淀质量为ng。再将
得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系正确的是
| A.c=1000b/11.2V | B.p=m+(Vc/125) |
| C.n=m+17Vc | D.(10/7)m<p<(17/9)m |
下列说法中正确的是
A.氯化钠的电子式是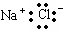 |
| B.按照不同分类标准,KAl(SO4)2属于强电解质、硫酸盐、酸式盐 |
| C.标准状况下,2.24 L C2H6中含有0.6 NA对共用电子对 |
| D.Mg、F2、H2O2依次是只有还原性、只有氧化性、既有氧化性也有还原性 |
设NA为阿伏加德罗常数的值。下列叙述错误的是
| A.常温常压下,0.17g NH3中含有的共用电子对数为0.1NA |
| B.常温常压下,1 L pH=1的稀H2SO4中含有的氢离子数为0.1NA |
| C.标准状况下,2.24 L C12与足量稀NaOH反应转移电子数为0.1NA |
| D.10 g由CaCO3与KHCO3组成的混合物中含有的碳原子数为0.1NA |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,5.6L CH4含C—H键数目为NA |
| B.常温常压下,100g17%H2O2水溶液含氧原子总数为NA |
| C.标准状况下,5.6L O2与适量Na加热反应,转移电子数一定为NA |
| D.常温常压下,14g乙烯与丙烯的混合气体,含碳原子总数为NA |
下列化学用语使用不正确的是
A.Na+的结构示意图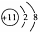 |
| B.纯碱的化学式为Na2CO3 |
C.聚乙烯的结构简式为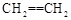 |
D.高氯酸(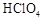 )中氯元素的化合价为+7 )中氯元素的化合价为+7 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.39g苯分子中含有的碳碳双键数为1.5NA |
| B.1molCH3COONa和少量CH3COOH溶于水所得中性溶液中,CH3COO-数目为NA |
| C.2.24LNH3中含共价键数目一定为0.3NA |
| D.5.6gFe投入100mL 3.5mol·L-1稀硝酸中,充分反应,转移电子总数为0.3 NA |