题目内容
下列物质中,既含离子键又含共价键的是
| A.HCl | B.NaOH | C.NaCl | D.O2 |
B
解析试题分析:离子键一般含有金属元素或铵根离子,共价键一般存在于非金属元素之间,所以答案选B
考点:考查化学键的相关知识点

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各含氧酸中,酸性最强的是
| A.HMnO4 | B.H2SeO3 | C.H3BO3 | D.H3PO4 |
关于离子键、共价键的各种叙述中,下列说法正确的是 ( )
| A.在离子化合物里,只存在离子键,没有共价键 |
| B.非极性键只存在于双原子的单质分子(如Cl2)中 |
| C.在共价化合物分子内,一定不存在离子键 |
| D.由不同元素组成的多原子分子里,一定只存在极性键 |
下列分子或离子中,含有孤对电子的是
A.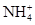 | B.CH4 | C.H2S | D.SiH4 |
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述不正确的是
A.NH4H的电子式为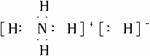 | B.NH4Cl的电子式为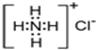 |
| C.NH4H含有极性共价键和离子键 | D.NH4H固体投入少量热水中,有两种气体生成 |
关于晶体的下列说法正确的是( )
| A.化学键都具有饱和性和方向性 |
| B.晶体中只要有阴离子,就一定有阳离子 |
| C.氢键具有方向性和饱和性,也属于一种化学键 |
| D.金属键由于无法描述其键长、键角,故不属于化学键 |

 ,每个晶胞中分摊2个钾原子
,每个晶胞中分摊2个钾原子 Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。