题目内容
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生。(2)第二份加足量NaOH溶液加热后,收集到0.04mol气体。(3)第三份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。综合上述实验,你认为以下结论正确的是( )
A.该混合液中一定含有:K+、NH4+、CO32-、SO42-、Cl-
B.该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl-
C.该混合液中一定含有:NH4+、CO32-、SO42-、Cl-,可能含K+
D.该混合液中:c(K+)≥0.2mol/L,c(CO32-)=0.2mol/L
【答案】D
【解析】
(1)加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
(2)0.04mol气体为氨气,溶液中一定含有NH4+,并且物质的量为0.04mol;
(3)2.33g沉淀为硫酸钡,6.27g沉淀为硫酸钡和碳酸钡的混合物;
再根据电荷守恒,得出一定存在钾离子,据此进行解答。
第一份加入AgNO3溶液有沉淀产生,与AgNO3溶液有沉淀产生的离子有:Cl-、CO32-、SO42-;
第二份加足量NaOH溶液加热产生气体,气体是氨气,故一定有铵离子0.04mol,溶液中一定含有NH4+,且NH4+离子的物质的量为0.04mol;
第三份加足量BaCl2溶液后得到沉淀质量为6.27g,再足量盐酸洗涤、干燥后,沉淀质量为2.33g为硫酸钡,其物质的量n(BaSO4)=![]() =0.01mol,则n(SO42-)= n(BaSO4)=0.01mol ;6.27g沉淀是硫酸钡和碳酸钡,m(BaCO3)=6.27g-2.33g=3.94g,碳酸钡的物质的量n(BaCO3)=
=0.01mol,则n(SO42-)= n(BaSO4)=0.01mol ;6.27g沉淀是硫酸钡和碳酸钡,m(BaCO3)=6.27g-2.33g=3.94g,碳酸钡的物质的量n(BaCO3)=![]() =0.02mol,则n(CO32-)= n(BaCO3)=0.02mol,所以原溶液中一定存在CO32-、SO42-,由于CO32-、SO42- 与Ba2+会形成沉淀不能大量共存,因此一定没有Ba2+; 再根据电荷守恒,2n(SO42-)+2n(CO32-)=2×0.01mol+2×0.02mol=0.06mol,n(NH4+)=0.04mol<0.06mol,正电荷总物质的量小于负电荷的物质的量,故原溶液中一定有K+,其物质的量至少为0.06mol-0.04mol=0.02mol;
=0.02mol,则n(CO32-)= n(BaCO3)=0.02mol,所以原溶液中一定存在CO32-、SO42-,由于CO32-、SO42- 与Ba2+会形成沉淀不能大量共存,因此一定没有Ba2+; 再根据电荷守恒,2n(SO42-)+2n(CO32-)=2×0.01mol+2×0.02mol=0.06mol,n(NH4+)=0.04mol<0.06mol,正电荷总物质的量小于负电荷的物质的量,故原溶液中一定有K+,其物质的量至少为0.06mol-0.04mol=0.02mol;
综合上述分析可以得出,一定存在的离子有:NH4+、K+、CO32-、SO42-,一定没有的离子Ba2+,可能存在Cl-,c(K+)≥0.02mol÷0.1L=0.2mol/L,c(CO32-)=0.02mol÷0.1L=0.2mol/L,c(SO42-)=0.01mol÷0.1L=0.1mol/L,c(NH4+)=0.04mol÷0.1L=0.4mol/L,故合理选项是D。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】滴定分析是一种操作简便、准确度很高的定量分析方法,它可广泛应用于中和滴定、氧化还原反应等滴定中。某研究性学习小组的同学利用滴定分析法进行下面两项定量分析。
(1)测定NaOH和Na2CO3的混合液中NaOH的含量。实验操作为先向混合液中加过量的BaCl2溶液使Na2CO3完全转化成BaCO3沉淀,然后用标准盐酸滴定(用酚酞作指示剂)。
①向混有BaCO3沉淀的NaOH溶液中直接滴入盐酸,则终点颜色的变化为____,为何此种情况能测出NaOH的含量?____。
②滴定时,若滴定管中的滴定液一直下降到活塞处才达到滴定终点,则能否由此准确地计算出结果?____,请说明理由:___。
(2)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.0000g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI=3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250 mL,然后用5.0×10-4mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O32-=2I-+S4O62-)。取用Na2S2O3的标准溶液应该用_____式滴定管。有关实验数值如表所示(第一次滴定终点的数据如图所示,请将读得的数据填入表中)。
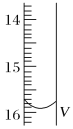
滴定次数 | 待测液的体积(mL) | 滴定前的读数(mL) | 滴定后的读数(mL) |
第一次 | 25.00 | 0.00 | V=_____ |
第二次 | 25.00 | 0.00 | 14.99 |
第三次 | 25.00 | 0.00 | 15.01 |
该碘盐中碘元素的百分含量为_____,下列操作中,会导致所测得的碘元素的百分含量偏大的是____。
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水