��Ŀ����
����Ŀ�����Ȼ�������ɫҺ�壬�۵�-33�����е�114����������������ڼ���ʱ��Ӧ���������Ʊ�SnCl4 �� SnCl4 ����ˮ�⣬�ڳ�ʪ�Ŀ����з��̡�ʵ���ҿ���ͨ����ͼװ���Ʊ�����SnCl4 ���г�װ��������
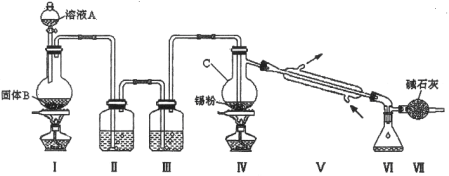
��1������C�������� ��
��2��װ�����з�����Ӧ�����ӷ���ʽΪ�� ��
��3��װ�����е�����Լ�Ϊ ��װ����������Ϊ ��
��4����װ������˳��Ϊ��һ��һ��һ��һ���������г�����SnCl4 �⣬�������ɵĺ����Ļ�����Ļ�ѧʽΪ ��
��5�����м��ȵ�����֮һ�Ǵٽ����������۷�Ӧ�����ȵ���һ����Ϊ ��
��6����������ȥ����11.9 g����Ӧ��������ƿ���ռ���23.8 g SnCl4 ����SnCl4 �IJ���Ϊ ��
���𰸡�
��1��������ƿ��
��2��MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��
��3�������Ȼ�����Һ����ֹ������ˮ�����������У�SnCl4ˮ�⣻
��4��ȱ��β������װ�ã�
��5��Sn��OH��4��SnO2�ȣ���6��91.2%��
��������
�����������װ��ͼ��֪װ����ӦΪ�Ʊ�����װ�ã��漰���ӷ�ӦΪMnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O��װ����Ϊ����ʳ��ˮ��װ����ΪŨ���ᣬ���������ӣ������������װ�����з�Ӧ����SnCl4������ȴ����װ�������ռ�����SnCl4����ˮ�⣬Ӧ��ֹ�����е�ˮ��������װ��������
Mn2++Cl2��+2H2O��װ����Ϊ����ʳ��ˮ��װ����ΪŨ���ᣬ���������ӣ������������װ�����з�Ӧ����SnCl4������ȴ����װ�������ռ�����SnCl4����ˮ�⣬Ӧ��ֹ�����е�ˮ��������װ��������
��1������C������Ϊ������ƿ���ʴ�Ϊ��������ƿ��
��2��װ������Ũ������MnO2�ڼ���ʱ������Ӧ����������������Ӧ�����ӷ���ʽΪ��MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+4H++2Cl-
Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��
��3�����������лӷ��ԣ���������ȡ�������к�������HCl�������������ӦǰҪ��ȥ�����װ�����е�����Լ�Ϊ��ȥHClͬʱ�����Լ����������ĵı���ʳ��ˮ��SnCl4����ˮ�⣬�ڳ�ʪ�Ŀ����з��̣�Ϊ�˷�ֹ��ˮ�⣬����Ҫ��ֹ��ˮ�⣮װ����������Ϊ��ֹ�����е�ˮ������������ʹSnCl4ˮ�⣬
�ʴ�Ϊ�������Ȼ�����Һ����ֹ������ˮ�����������У�SnCl4ˮ�⣻
��4��δ��Ӧ������û�г�ȥ��ȱ��β������װ�ã��ʴ�Ϊ��ȱ��β������װ�ã�
��5�����û��װ���������������к���ˮ���������������г�����SnCl4�⣬��������SnCl4ˮ������ĺ����Ļ�����Sn��OH��4��SnO2���ʴ�Ϊ��Sn��OH��4��SnO2�ȣ�
��6����������ȥ����11.9g����n��Sn��=0.1mol�������ϲ�����SnCl4�����ʵ�������m��SnCl4��=0.1mol��261g/mol=26.1g���Է�Ӧ����������ƿ���ռ���23.8gSnCl4����SnCl4�IJ���Ϊ![]() ��100%=91.2%���ʴ�Ϊ��91.2%��
��100%=91.2%���ʴ�Ϊ��91.2%��

 ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�