题目内容
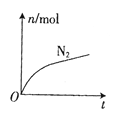
【题目】含铬(Cr)工业废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀。转化过程中,废水pH与Cr2O72-转化为Cr3+的关系如图1所示,实验室模拟工业电解法处理含铬废水的装置如图2所示。


请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是______________。
(2)写出下列反应的离子方程式:
①电解过程中的阴极反应式_________________;
②Cr2O72-转化为Cr3+的离子方程式________________。
【答案】(1)调节废水pH为1左右;
(2)①2H++2e-===H2↑;②6Fe2++Cr2O72-+14H+===6Fe3++2Cr3++7H2O。
【解析】
试题分析:(1)根据图1当pH=1左右时,Cr2O72-转化率最大,因此调节废水pH为1左右;
(2)碳棒接电源的负极,因此碳棒为阴极,根据电解原理,在阴极上得电子,发生还原反应,即2H+ + 2e- = H2↑;②铁棒作阳极,阳极反应式为Fe-2e-=Fe2+,Cr2O72-把Fe2+氧化成Fe3 + ,根据化合价升降法配平,其离子反应式:Cr2O72- + 6Fe2 + + 14H + =6Fe3 + + 2Cr3 + + 7H2O。

练习册系列答案
相关题目
【题目】已知:2NaAlO 2 + 3H2O +CO2→2Al(OH)3↓+Na2CO3。向含2molNaOH、 1 mol Ba(OH)2、2 molNaAlO 2的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量关系正确的是
选项 | A | B | C | D |
n(CO2)mol | 2 | 3 | 4 | 6 |
n(沉淀) mol | 2 | 2 | 3 | 3 |