题目内容
【题目】某金属氧化物的化学式为M2O3,电子总数为50,已知氧原子核内有8个中子,M2O3的相对分子质量为102,则M原子核内中子数为( )
A.10B.12C.14D.21
【答案】C
【解析】
氧原子核内有8个中子,则O的相对原子质量为16,M2O3的相对分子质量为102,M的相对原子质量=(102-16×3)÷2=27;已知M2O3电子总数为50,O原子核外有8个电子,则M原子核外有(50-8×3)÷2=13个电子,M原子核内中子数=27-13=14,答案为C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下列说法正确的是
A | B | C | D |
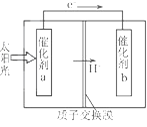
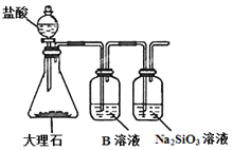
通电一段时间后,搅拌均匀,溶液的pH增大 | 此装置可实现 铜的精炼 | 盐桥中的K+ 移向FeCl3溶液 | 若观察到甲烧杯中石墨电极附近先变红,则乙烧杯中铜电极为阳极 |
|
|
|
|
A. A B. B C. C D. D