题目内容
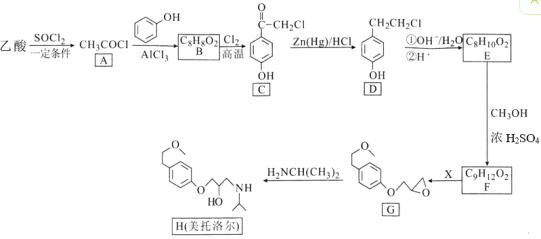
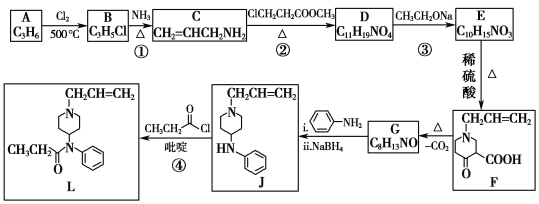
【题目】芬太尼类似物L具有镇痛作用,它的合成方法如图:
已知:
Ⅰ.![]() +Cl—R3
+Cl—R3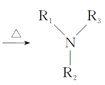 +HCl
+HCl
Ⅱ.R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
Ⅲ.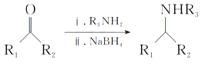 (R1、R2、R3、R4为氢原子或烃基)
(R1、R2、R3、R4为氢原子或烃基)
Ⅳ.RCH=CHR′![]() RCOOH+R′COOH,R、R′为烃基。
RCOOH+R′COOH,R、R′为烃基。
回答下列问题:
(1)A是一种烯烃,化学名称为__,其分子中最多有__个原子共面。
(2)B中官能团的名称为__、__。②的反应类型为__。
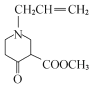
(3)③的化学方程式为__。
(4)碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳原子。用星号(*)标出F中的手性碳原子__。G的结构简式为__,符合以下条件的G同分异构体有___种。
①能发生银镜反应
②结构中只含有一个环,该环结构为![]() ,环上只有一个侧链
,环上只有一个侧链
(5)已知④有一定的反应限度,反应进行时加入吡啶(一种有机碱),其作用是__。
(6)参照上述合成路线,写出以环己烯(![]() )和乙醇为起始原料制备化合物
)和乙醇为起始原料制备化合物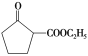 的合成路线(其他试剂任选)。___。
的合成路线(其他试剂任选)。___。
【答案】丙烯 7 碳碳双键 碳氯键 取代反应 
![]()
 +CH3OH
+CH3OH 
 8 吸收反应生成的HCl,提高反应转化率
8 吸收反应生成的HCl,提高反应转化率 ![]()
【解析】
A是一种烯烃,由A、B的分子式,C的结构简式,可知A为CH3CH=CH2,A发生取代反应生成B为ClCH2CH=CH2;由C的结构简式,以及反应②的条件,可知反应②发生信息I中取代反应,则D为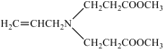 ;根据D的结构以及反应③的条件,可知反应③为信息II中的取代反应,结合E的分子式,可知E为
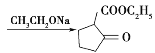
;根据D的结构以及反应③的条件,可知反应③为信息II中的取代反应,结合E的分子式,可知E为 ;E发生酯的水解反应生成F,对比F、J的结合,可知F脱羧生成G,G与苯胺脱去1分子水生成J,故G为
;E发生酯的水解反应生成F,对比F、J的结合,可知F脱羧生成G,G与苯胺脱去1分子水生成J,故G为 ;J与
;J与![]() 发生消去反应生成L。
发生消去反应生成L。
(1)根据分析可知A的结构简式为CH2=CH-CH3,A名称为:丙烯;旋转碳碳单键可以使甲基中1个H原子处于碳碳双键的平面结构内,分子中最多有7个原子共面;
(2)B为ClCH2CH=CH2,B中官能团有碳碳双键、碳氯键(氯原子),反应②是B的氨基中氢原子被-CH2CH2COOCH3替代,属于取代反应;
(3)反应③与信息II反应类似,化学方程式为:
![]()
 +CH3OH;
+CH3OH;
(4)用星号(*)标出F中的手性碳原子为: ;
;
根据分析可知G的结构简式为: ;
;
G的同分异构体满足:
①能发生银镜反应,说明含有—CHO;
②结构中只含有一个环,该环结构为![]() ,环上只有一个侧链,则其侧链可以为—CH=CH2CHO或—C(CHO)=CH2,环上有4种环境的氢,所以共有8种同分异构体;
,环上只有一个侧链,则其侧链可以为—CH=CH2CHO或—C(CHO)=CH2,环上有4种环境的氢,所以共有8种同分异构体;
(5)反应④为取代反应,生成有机物的同时可生成HCl,而吡啶呈碱性,可与HCl发生中和反应,使平衡正向移动,提高J的产率;
(6)由信息II可知,由![]() 反应得到
反应得到 ;
;![]() 用酸性高锰酸钾溶液氧化可以生成己二酸,己二酸与乙醇发生酯化反应得到
用酸性高锰酸钾溶液氧化可以生成己二酸,己二酸与乙醇发生酯化反应得到![]() ;合成路线流程图为:
;合成路线流程图为: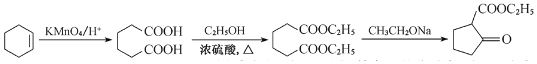 。
。

 学习实践园地系列答案
学习实践园地系列答案【题目】工业合成氨与制备硝酸一般可连续生产,流程如下:

(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g)![]() CO2(g)+H2(g)。
CO2(g)+H2(g)。
①t℃时,往1L密闭容器中充入0.2molCO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=___。
②保持温度不变,向上述平衡体系中再加入0.1molCO,当反应重新建立平衡时,水蒸气的总转化率α(H2O)=___。
(2)合成塔中发生反应为:N2(g)+3H2(g)![]() 2NH3(g) △H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1___573K(填“>”、“<”或“=”)。
2NH3(g) △H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1___573K(填“>”、“<”或“=”)。
T/K | T1 | 573 | T2 |
K | 1.00×107 | 2.45×105 | 1.88×103 |
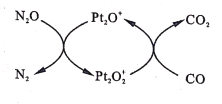
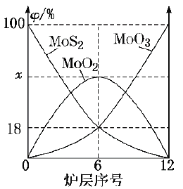
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3+5O2![]() 4NO+6H2O △H=-905kJ·mol-1 ,不同温度下NO产率如图所示。温度高于900℃时,NO产率下降的可能原因___。
4NO+6H2O △H=-905kJ·mol-1 ,不同温度下NO产率如图所示。温度高于900℃时,NO产率下降的可能原因___。

(4)吸收塔中反应为:3NO2+H2O![]() 2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因是___。
2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因是___。
(5)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:___。