题目内容
[化学—选修2:化学与技术](15分)
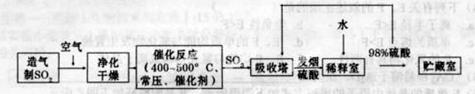
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到硫酸,如橡胶的硫化、表面活性剂“烷基苯硫酸钠”的合成,铅蓄电池的生产等。工业上生产硫酸的流程图如下:

请回答下列问题
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,已知1g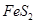 完全燃烧放出7.2kJ的热量
完全燃烧放出7.2kJ的热量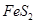 燃烧反应的热化学方程式_______ ______。
燃烧反应的热化学方程式_______ ______。
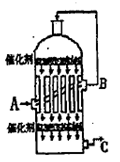
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用在具有多层催化剂且又热交换的________(填仪器名称)中进行反应。在如图Ⅰ所示的装置中, A处气体进入装置前需净化的原因是 。
(3)精制炉气(含有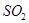 体积分数为7%、O2为11%、N2为82%)中
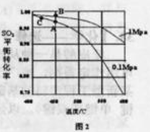
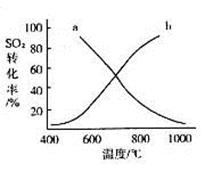
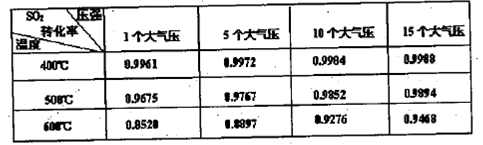
体积分数为7%、O2为11%、N2为82%)中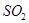 平衡 转化率与温度及压强关系如图2所示、在实际生产中,
平衡 转化率与温度及压强关系如图2所示、在实际生产中,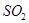 催化氧化反应的条件选择常压、
催化氧化反应的条件选择常压、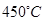 左右(对应图中A点):而没有选择
左右(对应图中A点):而没有选择 转化率更高的B或C点对应的反应条件,其原因分别是: 、 。
转化率更高的B或C点对应的反应条件,其原因分别是: 、 。
(4)已知:焙烧明矾的化学方程式4KAl(SO4)2?12H2O+3S═2K2SO4+2Al2O3+9SO2+48H2O。
焙烧711t明矾(M=474g/mol),若 的利用率为95%,可生产质量分数为98%的硫酸 t。(结果保留小数点后一位)
的利用率为95%,可生产质量分数为98%的硫酸 t。(结果保留小数点后一位)
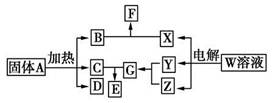
(5)除硫酸工业外,还有许多工业生产。下列相关的工业生产流程中正确的是
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到硫酸,如橡胶的硫化、表面活性剂“烷基苯硫酸钠”的合成,铅蓄电池的生产等。工业上生产硫酸的流程图如下:


请回答下列问题
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,已知1g
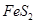 完全燃烧放出7.2kJ的热量
完全燃烧放出7.2kJ的热量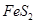 燃烧反应的热化学方程式_______ ______。
燃烧反应的热化学方程式_______ ______。 (2)为了有利于SO2转化为SO3,且能充分利用热能,采用在具有多层催化剂且又热交换的________(填仪器名称)中进行反应。在如图Ⅰ所示的装置中, A处气体进入装置前需净化的原因是 。
(3)精制炉气(含有
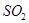 体积分数为7%、O2为11%、N2为82%)中
体积分数为7%、O2为11%、N2为82%)中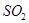 平衡 转化率与温度及压强关系如图2所示、在实际生产中,
平衡 转化率与温度及压强关系如图2所示、在实际生产中,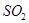 催化氧化反应的条件选择常压、
催化氧化反应的条件选择常压、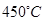 左右(对应图中A点):而没有选择
左右(对应图中A点):而没有选择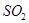 转化率更高的B或C点对应的反应条件,其原因分别是: 、 。
转化率更高的B或C点对应的反应条件,其原因分别是: 、 。
(4)已知:焙烧明矾的化学方程式4KAl(SO4)2?12H2O+3S═2K2SO4+2Al2O3+9SO2+48H2O。
焙烧711t明矾(M=474g/mol),若
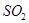 的利用率为95%,可生产质量分数为98%的硫酸 t。(结果保留小数点后一位)
的利用率为95%,可生产质量分数为98%的硫酸 t。(结果保留小数点后一位)(5)除硫酸工业外,还有许多工业生产。下列相关的工业生产流程中正确的是
| A.向装置中通入氮气且保持体积不变 |
| B.向装置中通入氧气且保持体积不变 |
| C.添加更多的催化剂 |
| D.降低温度,及时转移SO3 |
(第四空3分,其余2分)
(1)4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g)△H=-3456kJ/mol
(2)接触室 防止催化剂中毒;水蒸气对设备和生产有不良影响
(3)不选B点,因为压强越大对设备的投资越大,消耗的动能大,二氧化硫原料的转化率在1个大气压时已达97%左右,再提高压强二氧化硫的转化率提高余地很小,所以采用1个大气压;
不选C点,因为温度越低,二氧化硫的转化率虽然更高,但是催化剂的催化效率受到影响,450°C时,催化剂的催化效率最高,所以选择A点,不选C点。
(4)320.6
(5)B
(1)4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g)△H=-3456kJ/mol
(2)接触室 防止催化剂中毒;水蒸气对设备和生产有不良影响
(3)不选B点,因为压强越大对设备的投资越大,消耗的动能大,二氧化硫原料的转化率在1个大气压时已达97%左右,再提高压强二氧化硫的转化率提高余地很小,所以采用1个大气压;
不选C点,因为温度越低,二氧化硫的转化率虽然更高,但是催化剂的催化效率受到影响,450°C时,催化剂的催化效率最高,所以选择A点,不选C点。
(4)320.6
(5)B
试题分析:(1)FeS2的摩尔质量是120g/mol,则4mol的FeS2完全燃烧放出的热量为7.2kJ×120×4=3456kJ,所以热化学方程式为4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g)△H=-3456kJ/mol
(2)二氧化硫转化为三氧化硫在接触室中进行;A处气体中含有杂质易使催化剂中毒,且水蒸气对设备和生产有不良影响,所以在进入接触室之前需净化;
(3)在反应2SO2+O2?2SO3中,SO2转化率较高,工业上一般不采用更高的压强,因为压强越大对设备的投资越大,消耗的动能越大.SO2的转化率在1个大气压下的转化率已达到97%左右,在提高压强,SO2的转化率提高的余地很小;本反应为放热反应,工业生产中不采取较低的温度,因为温度越低,SO2的转化率虽然更高,但催化剂的催化作用会受影响,450℃时,催化剂的催化效率最高。所以选择A点。
(4)根据明矾焙烧的化学方程式及元素守恒规律得:4KAl(SO4)2?12H2O~9SO2~9H2SO4,二氧化硫的利用率为95%,设焙烧711t明矾可生成98%的硫酸质量为x:4KAl(SO4)2?12H2O~9H2SO4,
4×474 9×98
711t×95% x×98%
解得x=320.6t
(5)A、通入与反应无关的气体,体积不变,压强增大,对平衡无影响,且对反应装置无利,错误;B、向装置中通入氧气且保持体积不变,可以增大氧气的浓度,反应速率加快,平衡正向移动,二氧化硫的转化率提高,对生产有利,正确;C、催化剂只能加快反应速率,不能改变平衡,错误;D、转移SO3减少生成物浓度,平衡正向移动,二氧化硫转化率提高,但温度降低会使催化剂的活性降低,反应速率减慢,对生产不利,错误,答案选B。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
 L/L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式
L/L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式