题目内容
(12分)【化学——化学与技术】
工业上以黄铁矿为原料,采用接触法生产硫酸。请回答下列问题:
(1)煅烧黄铁矿的设备名称是__________,进料前必须将黄铁矿粉碎,目的是________。所得炉渣的用途有__________________________(填一种用途)。
(2)进入接触室前的气体必须经过净化处理,目的是防止________________________________。
(3)生产过程中,吸收三氧化硫常用的物质是_____________________________。
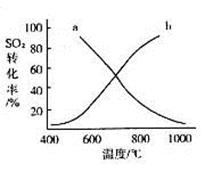
(4)温度变化与二氧化硫转化率的变化关系可用下图中的曲线______(填“a”或“b”)表示。
(5)工业上常用熟石灰和硫酸处理、回收尾气中的有害气体。反应的化学方程式为:
________________________________、_________________________________。
工业上以黄铁矿为原料,采用接触法生产硫酸。请回答下列问题:
(1)煅烧黄铁矿的设备名称是__________,进料前必须将黄铁矿粉碎,目的是________。所得炉渣的用途有__________________________(填一种用途)。
(2)进入接触室前的气体必须经过净化处理,目的是防止________________________________。
(3)生产过程中,吸收三氧化硫常用的物质是_____________________________。
(4)温度变化与二氧化硫转化率的变化关系可用下图中的曲线______(填“a”或“b”)表示。

(5)工业上常用熟石灰和硫酸处理、回收尾气中的有害气体。反应的化学方程式为:
________________________________、_________________________________。
(12分)
(1)沸腾炉(1分)增大接触面积。加快反应速率,使黄铁矿反应更充分(2分)
做水泥配料或炼铁原料(1分)
(2)催化剂中毒(2分)
(3)98.3%的浓硫酸(1分)
(4)a(1分)
(5)Ca(OH)2+SO2=CaSO3↓+H2O (2分)CaSO3+H2SO4 CaSO4+SO2↑+H2O(2分)
CaSO4+SO2↑+H2O(2分)
(1)沸腾炉(1分)增大接触面积。加快反应速率,使黄铁矿反应更充分(2分)
做水泥配料或炼铁原料(1分)
(2)催化剂中毒(2分)
(3)98.3%的浓硫酸(1分)
(4)a(1分)
(5)Ca(OH)2+SO2=CaSO3↓+H2O (2分)CaSO3+H2SO4
 CaSO4+SO2↑+H2O(2分)
CaSO4+SO2↑+H2O(2分)试题分析:(1)煅烧黄铁矿是在沸腾炉中与氧气反应,所以设备名称为:沸腾炉;将固体物质粉碎,可增大接触面积,加快反应速率,使黄铁矿反应更充分;炉渣中含Fe2O3,含铁量较高,经处理后常用作炼铁的原料。
(2)生成二氧化硫气体含有杂质,能使催化剂中毒,所以必须经过净化处理,防止催化剂中毒。
(3)为了防止酸雾的产生,用98.3%的浓硫酸吸收三氧化硫。
(4)因为SO2与O2反应是放热反应,温度升高,SO2的转化率减小,故可用曲线a表示。
(5)SO2被Ca(OH)2吸收,化学方程式为:Ca(OH)2+SO2=CaSO3↓+H2O;CaSO3再与硫酸反应,得到CaSO4并且回收SO2,化学方程式为:CaSO3+H2SO4
 CaSO4+SO2↑+H2O
CaSO4+SO2↑+H2O
练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
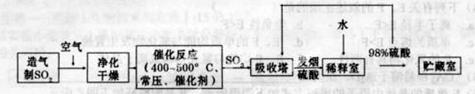

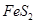 完全燃烧放出7.2kJ的热量
完全燃烧放出7.2kJ的热量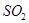 体积分数为7%、O2为11%、N2为82%)中
体积分数为7%、O2为11%、N2为82%)中 左右(对应图中A点):而没有选择
左右(对应图中A点):而没有选择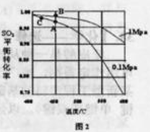
 N2O4的
N2O4的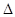 H<0
H<0