题目内容
16.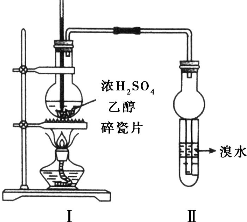 实验室制取乙烯的装置如图所示,试回答:
实验室制取乙烯的装置如图所示,试回答:(1)烧瓶中发生反应的化学方程式为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(2)实验中发现试管Ⅱ中溴水褪色,此现象能否说明一定有乙烯生产不能(填“能”或“不能”).试管中另一现象可证明确实有乙烯生成,该现象是液体分层,油状液体在下层;试管Ⅱ中溴水褪色能否说明是由于乙烯与溴水发生了加成反应不能(填“能”或“不能”).通过测定反应后溶液的pH可进一步证明是发生了取代反应还是加成反应,原因是若发生取代反应,生成HBr,水溶液pH明显减小;若发生加成反应,不能生成HBr,水溶液pH升高.
分析 (1)乙醇在浓硫酸做催化剂、脱水剂条件下生成乙烯和水;
(2)溴水褪色也可能是SO2所致,故应观看Ⅱ中液体是否分层,若分层且油状液体在下层,则说明一定有乙烯生成;若乙烯和溴水发生加成反应,则液体的pH升高;若发生取代反应,有HBr生成,水溶液的pH明显减小.
解答 解:(1)乙醇在浓硫酸做催化剂、脱水剂条件下生成乙烯和水,化学方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(2)溴水褪色也可能是SO2所致,乙烯与溴水反应生成有机物不溶于水,故应观看Ⅱ中液体是否分层,若分层且油状液体在下层,则说明一定有乙烯生成;若乙烯和溴水发生加成反应,则液体的pH升高;若发生取代反应,有HBr生成,水溶液的pH明显减小;
故答案为:不能;液体分层,油状液体在下层;不能;若发生取代反应,生成HBr,水溶液pH明显减小;若发生加成反应,不能生成HBr,水溶液pH升高.
点评 本题考查了乙烯的实验室制备及产物判断的实验设计,明确制备原理和乙烯性质是解题关键,注意实验设计的严密性,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
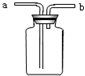 集气瓶被誉为“万能瓶”,如下图装置是其中的一种.当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排空气法收集气体.现若将被收集的气体从b口进入,则它可收集的气体为:①H2 ②O2 ③CO2( )
集气瓶被誉为“万能瓶”,如下图装置是其中的一种.当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排空气法收集气体.现若将被收集的气体从b口进入,则它可收集的气体为:①H2 ②O2 ③CO2( )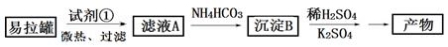
 。
。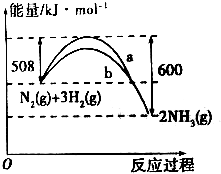 N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)?2NH3(g)达到平衡,测得反应放出热量为Q1kJ.
N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)?2NH3(g)达到平衡,测得反应放出热量为Q1kJ. Si+CO2↑
Si+CO2↑ .向Mg(HCO3)2溶液中加足量烧碱溶液:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O+CO32-
.向Mg(HCO3)2溶液中加足量烧碱溶液:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O+CO32-