题目内容
升高温度,下列数据不一定增大的是
A.化学反应速率 B.KNO3的溶解度S
B.KNO3的溶解度S
C.化学平衡常数K D.水的离子积常数Kw
C
【解析】
试题分析:A.在其它条件不变的情况下,升高温度化学反应速率 加快。不符合题意。错误。B.KNO3的溶解度S受温度的影响变化较大,升高温度,促进KNO3的溶解,所以KNO3的溶解度S增大。不符合题意。错误。C.化学平衡常数K只与温度有关。在其它条件不变的情况下,升高温度,化学平衡向吸热反应方向移动。如果可逆反应的正反应为放热反应,则升高温度,化学平衡向逆反应方向移动,K减小。如果可逆反应的正反应为吸热反应,则升高温度,化学平衡向正反应方向移动,K增大。所以升高温度化学平衡常数K。正确。D.水是弱电解质,升高温度,促进水的电离,水的离子积常数Kw增大。不符合题意。错误。
加快。不符合题意。错误。B.KNO3的溶解度S受温度的影响变化较大,升高温度,促进KNO3的溶解,所以KNO3的溶解度S增大。不符合题意。错误。C.化学平衡常数K只与温度有关。在其它条件不变的情况下,升高温度,化学平衡向吸热反应方向移动。如果可逆反应的正反应为放热反应,则升高温度,化学平衡向逆反应方向移动,K减小。如果可逆反应的正反应为吸热反应,则升高温度,化学平衡向正反应方向移动,K增大。所以升高温度化学平衡常数K。正确。D.水是弱电解质,升高温度,促进水的电离,水的离子积常数Kw增大。不符合题意。错误。
考点:考查温度对化学反应速率 、物质的溶解度S、化学平衡常数K、水的离子积常数Kw的影响。
、物质的溶解度S、化学平衡常数K、水的离子积常数Kw的影响。

四个体积相同的密闭容器中在一定的条件下发生反应: 2SO2+O2  2SO3,反应开始时,反应速率由大到小排列顺序正确的是
2SO3,反应开始时,反应速率由大到小排列顺序正确的是
容器 | 温度 | SO2(mol) | O2(mol) | 催化剂 |
甲 | 500℃ | 10 | 5 | - |
乙 | 500℃ | 10 | 5 | V2O5 |
丙 | 450℃ | 8 | 5 | - |
丁 | 500℃ | 8 | 5 | - |
A.乙>甲>丁>丙 B.乙>甲>丙>丁 C.甲>乙=丁>丙 D.乙>甲>丙=丁
在10 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
(1)该反应为 (填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K = 。
(3)能说明该反应达到化学平衡状态的是 (填字母)。
a.υ正(CO2)=υ正(H2) b.υ逆(CO)=υ逆(H2O)
c.υ逆(H2)=υ逆(H2O) d.υ正(H2)=υ逆(H2)
(4)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,测得 c(CO)=0.0080 mol·L-1 ,则CO2的转化率为 。
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
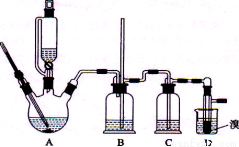
实验室用少量的溴水和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1) 烧瓶A中发生的主要的反应方程式: 。
(2) 安全瓶B可以防倒吸,并可以检查实验进行时试管D是否发生堵塞。请写出发生堵塞时瓶B中的现象: 。
(3) 在装置C中应加入 (填字母) ,其目的是
a.水 b.浓硫酸 c.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用 洗涤除去。(填字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(5)若产物中有少量副产物乙醚,可用 的方法除去。
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是 。

