题目内容
17.用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2•xH2O).有如下操作: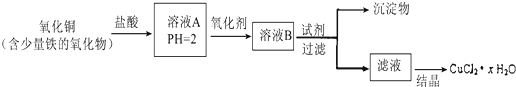
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解.
(1)能检验溶液A中Fe3+的试剂为①(填编号,下同)能检验溶液A中Fe2+的试剂
为⑤
①KSCN ②KSCN+Cl2 ③NaOH ④(NH4)2S ⑤KMnO4
(2)欲测定溶液A中的Fe2+的浓度,实验前,首先要配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、250mL容量瓶外,还需胶头滴管,下列滴定方式中(夹持部分略去),最合理的是a(填序号)

写出滴定反应的离子方程式5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
(3)若B溶液为25℃且pH=3,则B溶液的c(Fe3+)=4.0×10-5mol•L-1(已知25℃,Ksp[Fe(OH)3]=4.0×10-38).要得到较纯的产品,在B中加入试剂可选用CuO或Cu(OH)2 或CuCO3(填物质的化学式).
(4)为了测定制得的氯化铜晶体(CuCl2•xH2O)中x的值,某兴趣小组设计了如下实验方案:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为ng.据此计算得x=$\frac{80m-135n}{18n}$(用含m、n的代数式表示).
分析 向含少量铁的氧化铜固体中加入盐酸,盐酸和铁、氧化铜反应,发生的离子反应方程式为:Fe+2H+=Fe2++H2↑;CuO+2H+=Cu2++H2O,加入氧化剂A的目的是把亚铁离子氧化,根据除杂原则,不能引入新的杂质;试剂B应为调节溶液pH值,使Fe3+转化为Fe(OH)3,除去Fe3+,过滤除去沉淀,对滤液进行蒸发浓缩、冷却结晶、过滤得到氯化铜晶体.(1)溶液A中含有铜离子、亚铁离子,铁离子具有氧化性,与KSCN混合溶液变血红色,与氢氧根离子结合生成红褐色沉淀,与高锰酸钾溶液不反应;亚铁离子具有还原性,能被高锰酸钾氧化为三价铁,使高锰酸钾褪色;
(2)根据配制一定物质的量浓度的KMnO4溶液所需仪器和高锰酸钾的性质来分析;滴定反应:Mn元素的化合价由+7价降低为+2价,Fe元素的化合价由+2价升高为+3价,由电子守恒、电荷守恒、原子守恒解答;
(3)pH=3,根据水的电离平衡常数计算氢氧根离子浓度,Fe(OH)3存在平衡:Fe(OH)3(s)?Fe3+(aq)+3OH-(aq),根据Fe(OH)3的溶度积常数计算铁离子浓度,在制取过程中,不能引进杂质离子,据此来选择合适的试剂;
(4)CuCl2•xH2O中x的值的确定依据是加热前后的质量差即为减少的水的质量,据此来确定x.
解答 解:(1)溶液A中含有铜离子、亚铁离子,铁离子与KSCN混合溶液变红色,铁离子与氢氧根离子结合生成红褐色沉淀,但铜离子与氢氧根离子结合生成蓝色絮状沉淀干扰铁离子检验,铁离子与高锰酸钾溶液不反应,用KSCN无需用氯气,所以选择用KSCN是检验Fe3+最佳试剂,亚铁离子具有还原性,能被高锰酸钾氧化为三价铁,使高锰酸钾褪色,是检验溶液A中Fe2+的最佳试剂,
故答案为:①;⑤;
(2)配制一定物质的量浓度的KMnO4溶液需要的仪器有:天平、玻璃棒、烧杯、胶头滴管、250mL容量瓶,高锰酸钾具有强氧化性,必须放在酸式滴定管中,所以最合理的是a,滴定反应:Mn元素的化合价由+7价降低为+2价,Fe元素的化合价由+2价升高为+3价,由电子守恒、电荷守恒、原子守恒可知,离子反应为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,
故答案为:胶头滴管;a;5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
(3)若B溶液为25℃且pH=3,氢离子c(H+)=0.001mol/L,氢氧根离子c(OH-)=10-11mol/L,Fe(OH)3?Fe3++3OH-,25℃,Ksp[Fe(OH)3]=4.0×10-38,c(Fe3+)=$\frac{4.0×1{0}^{-38}}{(1{0}^{-11})^{3}}$=4.0×10-5mol•L-1,得到较纯的产品,需要调节pH使铁离子转化为沉淀,且不能引进杂质离子,选择的试剂可以是CuO、Cu(OH)2或Cu2(OH)2CO3,
故答案为:4.0×10-5;CuO或Cu(OH)2 或CuCO3;
(4)CuCl2•xH2O中x的值的确定依据是加热前后的质量差即为减少的水的质量,根据Cu元素守恒,则
CuCl2•xH2O~Cu(OH)2~CuO,
1 1
$\frac{m}{135+18x}$ $\frac{n}{80}$ $\frac{m}{135+18x}$=$\frac{n}{80}$ 解得:x=$\frac{80m-135n}{18n}$,
故答案为:$\frac{80m-135n}{18n}$.
点评 本题考查了物质的制备方案设计,侧重于考查学生的阅读获取信息能力、对工艺流程理解与实验条件控制、实验方案的评价、物质分离提纯除杂等实验操作能力,题目难度中等,要求学生要有扎实的实验基础知识和灵活应用信息解决问题的能力,注意基础知识的全面掌握.

| 元素 | 甲 | 乙 |
| 元素符号 | ①Na | ②Cl |
| 原子结构 示意图 |  | ③ 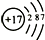 |
| 周期 | 三 | 三 |
| 族 | ④IA | VII A |
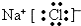 .
.(3)乙元素最高价氧化物对应水化物的化学式为HClO4.
(4)甲单质与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
| A. | 向某溶液中滴加BaCl2溶液,有白色沉淀生成,再滴加足量稀HNO3,沉淀不溶解,说明原溶液中一定含有Ag+ | |
| B. | 向某溶液中滴加浓NaOH溶液,加热,产生的气体使湿润的红色石蕊试纸变蓝色,说明原溶液中含NH4+ | |
| C. | 向某溶液中滴加足量稀盐酸,产生使澄清石灰水变浑浊的气体,说明原溶液中一定含CO32- | |
| D. | 用铂丝蘸取某溶液在无色火焰上灼烧,直接观察火焰颜色未见紫色,说明原溶液中不含K+ |
| A. | Na2CO3固体中混有少量NaHCO3:加入过量NaOH溶液,反应后加热蒸干 | |
| B. | FeCl2溶液中混有FeCl3:加入过量铁粉充分反应后过滤 | |
| C. | 铁粉中混有铝粉:加入过量烧碱溶液充分反应后过滤 | |
| D. | 氯气中混有少量氯化氢气体:将混合气体分别通过盛饱和食盐水和浓H2SO4的洗气瓶 |
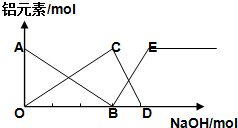
| A. | AB线表示Al3+的物质的量的变化 | B. | OC表示AlO2-的物质的量的变化 | ||
| C. | CD线表示Al(OH)3的物质的量的变化 | D. | BE线表示AlO2-的物质的量的变化 |
| A. | 两种元素构成的共价化合物分子中的化学键一定都是极性键 | |
| B. | 离子化合物中可以含有共价键,但共价化合物中一定不含离子键 | |
| C. | 非金属元素组成的化合物一定是共价化合物 | |
| D. | 非极性分子中,一定含有非极性键 |
| A. | Al(OH)3与稀盐酸反应:Al(OH)3+3H+═Al3++3H2O | |
| B. | AlCl3溶液中加入过量NH3•H2O:Al3++3OH-═Al(OH)3↓ | |
| C. | Al2(SO4)3溶液中加入少量Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ | |
| D. | NaAlO2溶液中加入少量稀H2SO4溶液:AlO2-+4H+═Al3++4H2O |
| A. | 氢键有方向性和饱和性,属于共价键 | |
| B. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| C. | 范德华力是一种分子间作用力,也是一种特殊的化学键 | |
| D. | 常温常压下,卤素单质从F2→I2由气态、液态到固态的原因是范德华力逐渐增大 |
