题目内容
金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)将一小块金属钠投入盛有水的烧杯中,发生反应的化学方程式为 :
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是 (填化学式,下同);适宜做耐火材料的是 ;
(3)金属铝既能与盐酸反应,又能与烧碱溶液反应,请写出金属铝与烧碱溶液反应的离子方程式: 。
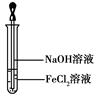
(4)取少量FeCl2溶液,按图所示操作,使其跟NaOH溶液反应。 可观察到试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色,请写出与上述现象相关的反应的化学方程式: 、 。
(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 (填序号)。
(1)将一小块金属钠投入盛有水的烧杯中,发生反应的化学方程式为 :
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是 (填化学式,下同);适宜做耐火材料的是 ;
(3)金属铝既能与盐酸反应,又能与烧碱溶液反应,请写出金属铝与烧碱溶液反应的离子方程式: 。
(4)取少量FeCl2溶液,按图所示操作,使其跟NaOH溶液反应。 可观察到试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色,请写出与上述现象相关的反应的化学方程式: 、 。

(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 (填序号)。
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
(1)2 Na + 2 H2O =2 NaOH + H2↑;
(2)Na2O2 (1分) Al2O3。
(3)2Al+2OH-+H2O ==2AlO2-+H2O
(4)FeCl2 + 2NaOH = Fe(OH)2↓+ 2NaCl 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(5)B
(2)Na2O2 (1分) Al2O3。
(3)2Al+2OH-+H2O ==2AlO2-+H2O
(4)FeCl2 + 2NaOH = Fe(OH)2↓+ 2NaCl 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(5)B
试题分析:(1)钠与水反应生成氢氧化钠和氢气,化学方程式为2 Na + 2 H2O =2 NaOH + H2↑;
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是Na2O2,适宜做耐火材料的是Al2O3,铁的氧化物适宜做颜料;
(3)金属铝与烧碱溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+H2O ==2AlO2-+H2O;
(4)氢氧化钠与氯化亚铁溶液反应先生成白色沉淀,迅速变成灰绿色,最终成为红褐色,发生的化学方程式为FeCl2 + 2NaOH = Fe(OH)2↓+ 2NaCl,4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(5)铁的还原性强于铜,所以铁先反应,只余铜或铁铜都余或铁铜都反应完都有可能,唯一不可能是有铁无铜,答案选B。

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目