题目内容
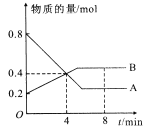
【题目】如图是部分短周期元素原子序数与最外层电子数之间的关系图,下列说法中正确的是( )

A.元素对应的离子半径:Z>X>R>W
B.简单氢化物的沸点:W>R>Y>Z
C.M、N、R、W的简单离子均能促进水的电离
D.Z、X、R、W的最高价氧化物对应的水化物均能与N的单质反应
【答案】D
【解析】
由部分短周期元素原子序数与最外层电子数之间的关系图,可知X为N元素、Y为O元素,Z为Na,M为Mg,N为Al,R为S,W为Cl。
A.对于电子层结构相同的离子,核电荷数越大离子半径越小;离子核外电子层越多离子半径越大,所以离子半径:r(S2-)>r(Cl-)>r(Na+)>r(Mg2+),A错误;
B.常温水为液态,其NH3、HCl、H2S均为气体,所以水的沸点最高,氨气分子之间存在氢键,沸点高于H2S、HCl,而HCl相对分子质量较大,分子间作用力较强,沸点高于H2S,所以简单氢化物沸点:水>氨气>氯化氢>硫化氢,B错误;
C.Mg2+、Al3+、S2-在溶液中均发生水解,促进水的电离,而Cl-不发生水解,不能促进水的电离,C错误;
D.Al是比较活泼的金属,能够与强酸、强碱溶液发生反应。Z、X、R、W的最高价氧化物对应的水化物分别为NaOH、HNO3、H2SO4、HClO4,NaOH是强碱,其余几种均为强酸,因此它们均能与Al发生反应,D正确;
故合理选项是D。

 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
NaCl溶于水 |
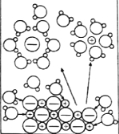
电解CuCl2溶液 |
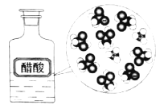
CH3COOH在水中电离 |
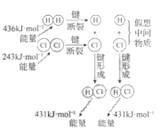
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D