题目内容
【题目】某混合物甲中含有明矾[KAl(SO4)2·12H2O]、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化。
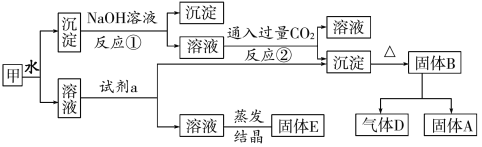
请回答下列问题:
(1)写出A、B、的化学式:A_____________, B_____________。
(2)试剂a最好选用______________。
A、NaOH溶液 B、稀盐酸
C、二氧化碳 D、氨水
(3)写出反应①的离子方程式:____________________。
(4)固体E可以作为复合性的化学肥料,E中所含物质的化学式为___________________。
【答案】Al Al2O3 D Al2O3+2OH-=2AlO2-+H2O K2SO4、(NH4)2SO4
【解析】
混合物甲含有KAl(SO4)212H2O、Al2O3和Fe2O3,由于KAl(SO4)212H2O溶于水,Al2O3和Fe2O3均不溶于水,混合物甲用水溶解后,溶液中含有KAl(SO4)2,沉淀是Al2O3和Fe2O3,向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,故沉淀为Fe2O3,溶液中含有NaAlO2,向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和NaHCO3,Al(OH)3受热分解生成B为Al2O3,电解熔融氧化铝得到气体D为O2,固体A为Al,向KAl(SO4)2溶液中加入试剂a也得到Al(OH)3,由于Al(OH)3溶于强碱,故试剂a最好是弱碱,故试剂a可为氨水,溶液中Al3+被沉淀,溶液中剩余的是K2SO4和(NH4)2SO4,经过蒸发、结晶得到的固体E中含有K2SO4和(NH4)2SO4,据此解答。
混合物甲含有KAl(SO4)212H2O、Al2O3和Fe2O3,由于KAl(SO4)212H2O溶于水,Al2O3和Fe2O3均不溶于水,混合物甲用水溶解后,溶液中含有KAl(SO4)2,沉淀是Al2O3和Fe2O3,向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,故沉淀为Fe2O3,溶液中含有NaAlO2,向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和NaHCO3,Al(OH)3受热分解生成B为Al2O3,电解熔融氧化铝得到气体D为O2,固体A为Al,向KAl(SO4)2溶液中加入试剂a也得到Al(OH)3,由于Al(OH)3溶于强碱,故试剂a最好是弱碱,故试剂a可为氨水,溶液中Al3+被沉淀,溶液中剩余的是K2SO4和(NH4)2SO4,经过蒸发、结晶得到的固体E中含有K2SO4和(NH4)2SO4,
(1)由上述分析可知,A为Al,B为Al2O3;
故答案为:Al;Al2O3;
(2)由上述分析可知,KAl(SO4)2溶液中加入试剂a也得到Al(OH)3,由于Al(OH)3溶于强碱,故试剂a最好是弱碱,故试剂a可为氨水;
故答案为;D;
(3)由上述分析可知,反应①为Al2O3与NaOH溶液反应,生成NaAlO2和水,其离子方程式为Al2O3+2OH-=2AlO2-+H2O;
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(4)向溶液中加入的试剂a应沉淀铝离子,应向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4和(NH4)2SO4,固体E可以作为复合性的化学肥料,E中所含物质的化学式为K2SO4和(NH4)2SO4;
故答案为:K2SO4、(NH4)2SO4。

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案【题目】有A、B、C、D四种易溶于水的白色固体,分别由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A______;D______。
(2)写出下列反应的离子方程式:
①B+D→:______;
③C+HCl→气体:______。
(3)在作实验反思时,有同学提出:如果溶液中同时存在![]() 和
和![]() ,
,![]() 会对
会对![]() 的检验产生干扰。为了确定该溶液中是否存在
的检验产生干扰。为了确定该溶液中是否存在![]() ,该小组同学进行了如下探究实验:
,该小组同学进行了如下探究实验:
实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
第一步 | 向溶液中滴加过量的 | 除去 ______的干扰 | 略 |
第二步 | 向第一步实验后的溶液中滴加______ | 检验 ______的存在 | 略 |