题目内容
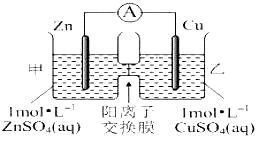
【题目】在关于下图所示的原电池中,正确的是
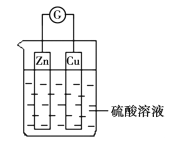
A. Zn被还原
B. 锌片上的电子经导线流向铜片
C. 该原电池运行一段时间后铜片的质量将增加
D. 该原电池将电能转变为化学能
【答案】B
【解析】
该装置为原电池,锌是负极,铜是正极,以此分析。
A、锌比铜活泼,铜是正极,锌是负极,锌失电子发生氧化反应,即锌被氧化,A错误;
B、锌片上的电子经导线流向铜片,B正确;
C、铜是正极,铜电极的反应是溶液中的H+得电子生成氢气,铜片的质量没有改变,C错误;
D、该装置将化学能转化为电能,D错误,
答案选B。
点晴:掌握原电池的工作原理是解答的关键,原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目