��Ŀ����
����Ŀ��ijѧϰС���о���Һ��Fe2+���ȶ��ԣ���������ʵ�飬�۲죬��¼�����

ʵ���
���� | 0 min | 1min | 1h | 5h |
FeSO4 | ����ɫ | �ۺ�ɫ | ��ɫ | ���ɫ |
(NH4)2Fe(SO4)2 | ������ɫ | ����ɫ | ��ɫ | �ۺ�ɫ |
��1������(NH4)2Fe(SO4)2��ҺpHС��FeSO4��ԭ����_______���û�ѧ�����ʾ������Һ���ȶ��ԣ�FeSO4_______(NH4)2Fe(SO4)2������������� ��
��2����ͬѧ���ʵ���������Һ���ȶ��Բ��������(NH4)2Fe(SO4)2��Һ�е�NH4+������Fe2+����ΪNH4+���л�ԭ�ԡ�����ʵ����˸ù۵㣬��ȫ��ʵ�顣
���� | ���� |
ȡ_______����_______���۲졣 | ��ʵ�����(NH4)2Fe(SO4)2��Һ������ͬ�� |
��3����ͬѧ���ʵ���������Һ���ȶ��Բ�������Һ���Բ�ͬ���£�����ʵ��ֱ�����0.80 mol��L��1 pHΪ1��2��3��4��FeSO4��Һ���۲죬����pH��1��FeSO4��Һ��ʱ�������Ա仯��pHԽ��FeSO4��Һ��Ƶ�ʱ��Խ�̡�
������ʾ����������Һ�д��ڷ�Ӧ 4Fe2+��O2��10H2O ![]() 4Fe(OH)3��8H+
4Fe(OH)3��8H+
��ʵ��III����ͬѧ�ɵó��Ľ�����_______��ԭ����_______��
��4����һ���о���ˮ��Һ��Fe2+�������������ⶨͬŨ��FeSO4��Һ�ڲ�ͬpH�����£�Fe2+������������ʱ��Ĺ�ϵ��ͼ��ʵ���������Һ�¶ȼ����ޱ仯������Ӧ���ڣ��������ʶ��������ԭ�������_____��
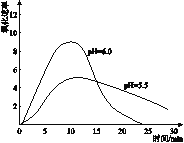
��5���ۺ�����ʵ�飬��ǿFe2+�ȶ��ԵĴ�ʩ��_______��
���𰸡�NH4+��H2O![]() NH3��H2O��H+ �� ȡ2 mL pH��4.0��0.80 mol��L��1 FeSO4��Һ ��2��0.01 mol��L��1 KSCN��Һ ��ҺpHԽС��Fe2+Խ�ȶ� ��Һ�д���ƽ��4Fe2+��O2��10H2O
NH3��H2O��H+ �� ȡ2 mL pH��4.0��0.80 mol��L��1 FeSO4��Һ ��2��0.01 mol��L��1 KSCN��Һ ��ҺpHԽС��Fe2+Խ�ȶ� ��Һ�д���ƽ��4Fe2+��O2��10H2O ![]() 4Fe(OH)3��8H+�� c��H+����ƽ�����������ǿ��Fe2+���ȶ� ���ɵ�Fe(OH)3�Է�Ӧ�д����� ��һ��������ܷⱣ��
4Fe(OH)3��8H+�� c��H+����ƽ�����������ǿ��Fe2+���ȶ� ���ɵ�Fe(OH)3�Է�Ӧ�д����� ��һ��������ܷⱣ��
��������
��1����NH4��2Fe��SO4��2��Һ��FeSO4�е�Fe2+Ũ����ͬ�����У�NH4��2Fe��SO4��2����Ũ�Ƚϸߵ�NH4+��ͨ�������е���ɫ�仯��������
��2��������Ҫ��֤����Һ���ȶ��Բ����Ƿ������ڣ�NH4��2Fe��SO4��2��Һ�е�NH4+������Fe2+���£����ݿ��Ʊ�������֪��Ӧ������NH4+���Ӱ�������������Ӱ�����ؾ�����һ�£��ݴ˷�����
��3����ʵ����֪����Һ��pHԽС����Һ������Խǿ����Fe2+Խ�ȶ�����������Һ�д��ڷ�Ӧ4Fe2++O2+10H2O4Fe��OH��3+8H+������ƽ����ƶ���������
��4������Ӱ�췴Ӧ���ʵ�������Ũ�ȡ�ѹǿ���¶Ⱥʹ�����������
��5����������ʵ����������
��1����NH4��2Fe��SO4��2��Һ��FeSO4�е�Fe2+Ũ����ͬ������NH4��2Fe��SO4��2��Һ�к���Ũ�Ƚϸߵ�NH4+��NH4+ˮ�������ԣ����£�NH4��2Fe��SO4��2�е�pH��С��ͨ�������е���ɫ�仯��֪��NH4��2Fe��SO4��2�е�Fe2+�����������ʸ���������Һ���ȶ��ԣ�FeSO4<��NH4��2Fe��SO4��2���ʴ�Ϊ��NH4++H2O![]() NH3H2O+H+��<��
NH3H2O+H+��<��
��2��������Ҫ��֤����Һ���ȶ��Բ����Ƿ������ڣ�NH4��2Fe��SO4��2��Һ�е�NH4+������Fe2+���£����ݿ��Ʊ�������֪��Ӧ������NH4+���Ӱ�������������Ӱ�����ؾ�����һ�£���Ӧȡ2mLpH=4.0��0.80molL-1FeSO4��Һ���Թ��У���2��0.01molL-1KSCN��Һ�������۲쵽��������ʵ����У�NH4��2Fe��SO4��2��Һ������ͬ����˵���������벻��ȷ���ʴ�Ϊ��ȡ2mLpH=4.0��0.80molL-1FeSO4��Һ����2��0.01molL-1KSCN��Һ��
��3����ʵ����֪����Һ��pHԽС����Һ������Խǿ����Fe2+Խ�ȶ�����������Һ�д��ڷ�Ӧ4Fe2++O2+10H2O![]() 4Fe��OH��3+8H+����Һ��pHԽС����������Ũ��Խ��ƽ�����ƣ���Fe2+�����������ƣ��ʴ�Ϊ����ҺpHԽС��Fe2+Խ�ȶ�����Һ�д���ƽ��4Fe2++O2+10H2O
4Fe��OH��3+8H+����Һ��pHԽС����������Ũ��Խ��ƽ�����ƣ���Fe2+�����������ƣ��ʴ�Ϊ����ҺpHԽС��Fe2+Խ�ȶ�����Һ�д���ƽ��4Fe2++O2+10H2O![]() 4Fe��OH��3+8H+��c��H+����ƽ�����������ǿ��Fe2+���ȶ���
4Fe��OH��3+8H+��c��H+����ƽ�����������ǿ��Fe2+���ȶ���
��4��Ӱ�췴Ӧ���ʵ�������Ũ�ȡ�ѹǿ���¶Ⱥʹ�������ͬһ�������ϵ�Ũ��FeSO4��Һ��ͬ����Ӧ���ŷ�Ӧ�Ľ��У�Fe2+��Ũ�ȼ�С���ʲ���Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻���˷�ӦΪ��Һ�еķ�Ӧ����ѹǿ�Դ˷�Ӧ������Ӱ�죻���˷�Ӧ���¶Ȳ��䣬����Ӱ�췴Ӧ���ʵ�ֻ�д�������Ψһ�Ŀ���ԭ�������ɵ�Fe��OH��3�Է�Ӧ�д����ã��ʴ�Ϊ�����ɵ�Fe��OH��3�Է�Ӧ�д����ã�
��5����������ʵ���֪������һ�������������Fe2+�����������Ǹ��������ܷⱣ�棬�ʴ�Ϊ������һ�������ᣬ�ܷⱣ�档