题目内容
5.一定温度下,两个恒容密闭容器中分别发生反应:①H2(g)+I2(g)═2HI(g); ②C(s)+H2O(g)═CO(g)+H2(g),下列状态能表明两反应都达到平衡状态的是( )a.各物质的浓度不变;
b.容器内气体压强不变;
c.容器内气体密度不变;
d.容器内气体颜色不变;
e.各组分的物质的量分数或质量分数不变;
f.混合气体的平均分子量不变.
| A. | ae | B. | aef | C. | abc | D. | ac |
分析 当反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量不变,注意①反应是一个反应前后气体体积不变的化学反应,所以不能用压强判断平衡.
解答 解:a.各物质的浓度不变,说明①②中各物质的量不变,都达平衡状态,故a正确;
b.容器内气体压强不变,①压强始终不变,所以压强不变无法判断①是否达到平衡状态,故b错误;
c.容器内气体密度不变,由于①反应的两边气体的体积相同且都是气体,容器的容积不变,所以密度始终不变,无法判断①是否达到平衡状态,故c错误;
d.容器内气体颜色不变,由于②反应容器内气体颜色始终不变,故d错误;
e.各组分的物质的量分数或质量分数不变,说明①②中各物质的量不变,都达平衡状态,故e正确;
f、反应①中气体的质量和物质的量始终不变,混合气体的平均分子量始终不变,所以平均相对分子质量不变不能说明反应①达到平衡状态,故f错误;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意反应前后气体体积不变的化学反应不能用压强来判断是否达到平衡状态.

练习册系列答案
相关题目
15.各组性质比较的表示中,正确的是( )
| A. | 沸点:Cl2<2<Br2<I2 | B. | 沸点:HF<HCl<HBr<HI | ||
| C. | 氧化性:F2<Cl2<Br2<I2 | D. | 还原性:HF<HCl<HBr<HI |
16.下列说法不正确的是( )
| A. | 金属单质和盐溶液的反应不一定是置换反应 | |
| B. | “水滴石穿”是因为CaCO3与CO2、水发生了化学反应 | |
| C. | 纯碱是制作面包等糕点的膨松剂,也是治疗胃酸过多的一种药剂 | |
| D. | 少量液溴可用水封存,防止溴挥发 |
13.为了测定酸碱反应的反应热,计算时至少需要的数据是( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量
⑤反应前后溶液温度变化 ⑥操作所需的时间.
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量
⑤反应前后溶液温度变化 ⑥操作所需的时间.
| A. | ①②③⑤ | B. | ①③④⑥ | C. | ③④⑤⑥ | D. | 全部 |
10.下列关于二氧化硫的说法正确的是( )
| A. | 二氧化硫是无色无味无毒的气体 | B. | 二氧化硫不是形成酸雨的主要成分 | ||
| C. | 二氧化硫可以与水反应形成硫酸 | D. | 二氧化硫可以使品红褪色 |
17.下列叙述中,可以表明N2+3H2═2NH3的反应达到平衡状态的是( )
| A. | 1mol N≡N键断裂的同时,有3mOLH-H键形成 | |
| B. | 1molN≡N键断裂的同时,有3molH-H键断裂 | |
| C. | 1molN≡N键断裂的同时,有6molN-H键形成 | |
| D. | 1molN≡N键断裂的同时,有6molN-H键断裂 |
13.检验某未知溶液中是否含有SO${\;}_{4}^{2-}$的下列操作中最合理的是( )
| A. | 加入硝酸酸化的Ba(NO3)2 | B. | 先加HNO3酸化,再加Ba(NO3)2溶液 | ||
| C. | 先加盐酸酸化,再加BaCl2溶液 | D. | 加入盐酸酸化了的BaCl2溶液 |
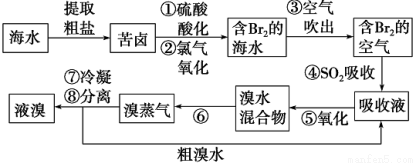
 吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下: