题目内容
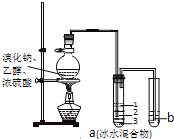
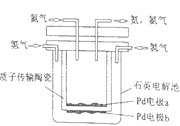
【题目】原电池是将_____能转化成_____能的一种装置。一种利用原电池原理制备NH3的装置如图所示,陶瓷在高温时可以传输H+。该设备中,电极____(填“a”或“b”)作负极,其电极反应式为:_____。当电路中通过1.2mol的电子时,可生成NH3____mol。
【答案】化学 电 b H2-2e-=2H+ 0.4
【解析】
根据原电池原理分析解答,根据电极反应式进行相关计算。
根据原电池原理分析知,原电池是将化学能转化成电能的一种装置;如图所示,总反应为:3H2+N2=2NH3,氢气发生氧化反应,作负极,氢气在电极b上反应,则电极b作负极;根据题给信息,反应过程中有H+生成,则负极反应为:H2-2e-=2H+;根据负极反应式知1.2mol电子转移时,消耗0.6mol氢气,根据总方程式得,消耗0.6mol氢气时生成氨气的物质的量为![]() ;故答案为:化学;电;b;H2-2e-=2H+;0.4。
;故答案为:化学;电;b;H2-2e-=2H+;0.4。

【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A. I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B. II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
【题目】一名同学把4.48 L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8 mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
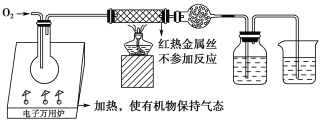
实验结束后发现无水CuSO4变蓝,干燥管和洗气瓶共增重18 g,澄清石灰水变浑浊后又恰好变澄清。请根据实验回答下列问题:
(1)O2要过量的原因是:________________。
(2)若该有机物只含C、H两种元素,且不含任何官能团,也不含脂环,则该有机物的分子式为________,它可能属于________(填序号)。
A.烷烃 B.苯的同系物 C.芳香烃 D.烃的衍生物
该物质可能的结构简式为_____________________。
(3)若该有机物分子中含有一个氧原子,则它可能是哪几类物质?请各举一例,填写在下表中:
物质种类 | 实例(写结构简式) |
_________ | _________ |
_________ | _________ |
_________ | _________ |