题目内容
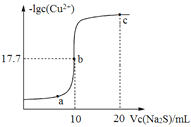
【题目】某温度下,向10 mL 0.1 mol/LCuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加过程中溶液中lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是
已知:lg2=0.3,Ksp(ZnS)=3×10-25 mol2/L2。
A. a、b、c三点中,水的电离程度最大的为b点
B. Na2S溶液中:c(H+)+c(HS-)+c(H2S)= c(OH-)
C. 该温度下Ksp(CuS)=4×10-36 mol2/L2
D. 向100 mL Zn2+、Cu2+浓度均为10-5 molL-1的混合溶液中逐滴加入10-4 molL-1的Na2S溶液,Zn2+先沉淀
【答案】C
【解析】A、CuCl2和Na2S发生CuCl2+Na2S=CuS↓+2NaCl,b点时两者恰好完全反应,a点时CuCl2过量,CuCl2属于强酸弱碱盐,Cu2+水解,促进水的电离,c点时Na2S过量,S2-水解,促进水的电离,因此水的电离程度最大的不是b点,故A错误;B、根据质子守恒,则有c(H+)+c(HS-)+2c(H2S)=c(OH-),故B错误;C、CuS(s) ![]() Cu2+(aq)-+S2-(aq),在b点时c(Cu2+)=c(S2-)=10-17.7,Ksp(Cu2S)=10-17.7×10-17.7=10-35.4,已知lg2=0.3,
Cu2+(aq)-+S2-(aq),在b点时c(Cu2+)=c(S2-)=10-17.7,Ksp(Cu2S)=10-17.7×10-17.7=10-35.4,已知lg2=0.3,
Ksp(CuS)=(10-0.3)2×10-36=4×10-36 mol2/L2,故C正确;D、Zn2+出现沉淀,需要c(S2-)=Ksp(ZnS)/c(Zn2+)=3×10-25/10-5mol·L-1=3×10-20mol·L-1,Cu2+出现沉淀,需要c(S2-)= Ksp(CuS)/c(Cu2+)=4×10-36/10-5mol·L-1=4×10-31mol·L-1,因此Cu2+先沉淀,故D错误。

 阅读快车系列答案
阅读快车系列答案