题目内容
12.下列有关说法中错误的是( )| A. | 氢氟酸不能盛放在玻璃试剂瓶中 | |
| B. | 玻璃、水晶、陶瓷的主要成分均是硅酸盐 | |
| C. | 灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO2能与NaOH反应 | |
| D. | 由沙子制备光伏材料时的反应之一为SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ |
分析 A.HF与二氧化硅反应;
B.水晶的成分为二氧化硅;
C.SiO2能与NaOH反应生成硅酸钠和水;
D.光伏材料为Si,利用C还原二氧化硅制备.
解答 解:A.HF与二氧化硅反应,则氢氟酸不能盛放在玻璃试剂瓶中,可利用塑料瓶,故A正确;
B.水晶的成分为二氧化硅,而玻璃、陶瓷的主要成分均是硅酸盐,故B错误;
C.SiO2能与NaOH反应生成硅酸钠和水,则灼烧NaOH固体时不能使用瓷坩埚,使用铁坩埚,故C正确;
D.光伏材料为Si,利用C还原二氧化硅制备,发生SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故D正确;
故选B.
点评 本题考查物质的性质,为高频考点,把握物质的性质、性质与用途、试剂的保存等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
2.下列化合物的核磁共振氢谱中出现三组峰的是( )
| A. | 2-甲基-2-丁烯 | B. | 苯酚 | ||
| C. | 2,2,3,3-四甲基戊烷 | D. | 3,4-二甲基己烷 |
3.在某K2SO4和Fe2(SO4)3的混合溶液中,Fe3+摩尔浓度为0.1摩/升,SO42-摩尔浓度为0.3摩/升,则K+的物质的量浓度为( )摩/升.
| A. | O.6 | B. | 0.3 | C. | 0.2 | D. | 0.15 |
7.下列实验操作或记录正确的是( )
| A. | 用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28 mL | |
| C. | 用两只250 mL的容量瓶配制0.1 mol•L-1500 mLNaOH溶液 | |
| D. | 常温常压下测得1 mol N2的质量为28 g |
17.已知As、Br在周期表的同一周期.下列关系正确的是( )
| A. | 原子半径:As>Cl>P | B. | 热稳定性HCl>HBr>AsH3 | ||
| C. | 酸性:H3AsO4>H2SO4>H3PO4 | D. | 还原性:S2->Cl->Br- |
4.25℃时,0.1mol•L-1的CH3COOH溶液和0.1mol•L-1的NaOH溶液等体积混合,则下列说法正确的是( )
| A. | 对混合液加热,溶液的pH减小 | B. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(CH3COO-)+c(OH-)=c(Na+) | D. | c(CH3COOH)+c(CH3COO-)=0.1mol•L-1 |
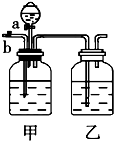 实验室用下列反应制取CO2和CO:H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,然后用如图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液.试回答下列各题:
实验室用下列反应制取CO2和CO:H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,然后用如图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液.试回答下列各题: