��Ŀ����
����Ŀ���ơ���������������Ҫ�Ľ�������ش�
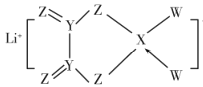
(1)�뻭���Ƶ�ԭ�ӽṹʾ��ͼ_______ �������Ƶ�ԭ�ӽṹʾ��ͼ�ɵó��Ƶ���Щ���ʣ�(д��һ��)_________��
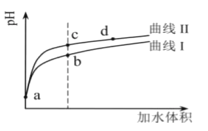
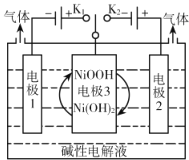
(2)�����ֽ����Ľ��������ǿ������˳����_________ ��
(3)С�������Ͷ��ˮ�У�������Ӧ�Ļ�ѧ����ʽΪ_______________���ɹ۲쵽��ʵ��������_________ (����ĸ)��
a.�Ƴ���ˮ�� b.���۳�С�� c.С���Ĵ��ζ�d.ˮ���ɫ
(4)����ϡ���ᷴӦ�����ӷ���ʽΪ_________________________________��
���𰸡�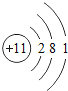 ǿ��ԭ�� Na��Al��Fe 2Na + 2H2O=2NaOH + H2�� bc 2Al +6H+=2Al3++ 3H2��
ǿ��ԭ�� Na��Al��Fe 2Na + 2H2O=2NaOH + H2�� bc 2Al +6H+=2Al3++ 3H2��
��������
(1)��ԭ�Ӻ�����11���ӣ������С��4�����ӵ�ԭ����ʧȥ���ӣ�
(2)��Ͻ����˳����жϣ�
(3)Na���ܶ�С��ˮ���Ƶ��۵�ϵͣ��ƺ�ˮ��Ӧ����NaOH������ͬʱ�ų������ȣ����������������Ĵ��ζ���
(4)Al����ϡ����������������������
(1)��ԭ�Ӻ�����11���ӣ�����ԭ�ӵĽṹʾ��ͼ�� �������ֻ��1�����ӣ���ʧ���ӣ�����ǿ��ԭ�ԣ�
�������ֻ��1�����ӣ���ʧ���ӣ�����ǿ��ԭ�ԣ�
(2)�ɽ����˳���֪��Na��Al��Fe�Ľ�����ǿ��˳��ΪNa��Al��Fe��
(3)Na���ܶ�С��ˮ�������ƻḡ��ˮ���ϣ��Ƶ��۵�ϵͣ��ƺ�ˮ��Ӧ����NaOH������ͬʱ�ų�������ʹ�����ڷ���˻˻�����������������������Ĵ��ζ�������NaOH������Һ�ʼ��ԣ�����ˮ��û�еμӷ�̪������Һ����ɫ���ʷ�����Ӧ�Ļ�ѧ����ʽΪ2Na + 2H2O=2NaOH + H2����ʵ��������ȷ����bc��
(4)Al����ϡ����������������������������Ӧ�����ӷ���ʽΪ2Al +6H+=2Al3++ 3H2����

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�����Ŀ��Ϊ�����ú��������,�����Ȱ�úת��ΪCO��H2���ٽ�����ת��Ϊ�״���ijʵ����Ա��һ���¶���2L���ܱ������У�����һ������H2��CO��������Ӧ��2H2(g)+CO(g)![]() CH3OH(g)���ⶨ�IJ���ʵ���������£�
CH3OH(g)���ⶨ�IJ���ʵ���������£�
t/s | 0 | 500 | 1000 |
c(H2)/ mol.L-1 | 5.00 | 3.52 | 2.48 |
c(CO)/ mol.L-1 | 2.50 |
(1)��500s����H2��ʾ�Ļ�ѧ��Ӧ������________________��
(2)��1000s����CO��ʾ�Ļ�ѧ��Ӧ������________________��1000sʱCO��ת������________��
(3)��500sʱ���ɵļ״���Ũ����________