��Ŀ����
��10�֣�
�� Ũ��Ϊ0.1 mol��L��1�����ᡢ���ᡢ����������Һ���Իش�
(1)������Һ��c(H��)����Ϊa mol��L��1��b mol��L��1��c mol��L��1�����ɴ�С��˳����________��
(2)��ȫ�к�һ����NaOH��Һʱ������������������������V1L��V2L��V3L�����С��ϵΪ__________________________________��
(3)��п��Ӧ��ʼʱ�������������ʷֱ�Ϊv1��v2��v3�����ɴ�С��˳����________��
�� c(H+)��ͬ�����ᡢ���ᡢ����������Һ���Իش�
(1)������Һ����ˮϡ�������Ϊԭ����10��, c(H+)����Ϊa mol��L��1��b mol��L��1��c mol��L��1�����ɴ�С��˳����_______��
(2)������Һ�����ͬʱ,ͬʱ������ͬ��п,��������ͬ���ʵ���������������ʱ��ֱ�Ϊt1��t2��t3�����С��ϵ��___________.
���bac ��V1=2V2=V3 ��bac ���c��a="b" ��t1=t2��t3
���������������.
��1������c(H��)=0.1mol/L������c(H��)=0.2mol/L������c(H��)��0.1mol/L����b��a��c��
��2��Ũ����ͬ�Ĵ��ᣬ���ᣬ���ᣬ���ߵ���Һ��H+Ũ�ȹ�ϵΪ���������ᣬ��Ϊ����Ϊ��Ԫ�ᣬH+Ũ��Ϊ��������H+Ũ�ȵ�2����������Ϊ���ᣬ���ֵ�������H+Ũ������С�ģ����ܵ�H+��Ũ�ȹ�ϵΪ����=������ᣬ���������Ϊǿ����ȫ���룬�����к�NaOH�������������ϵΪ����=������ᣬ��V1=2V2=V3��
��3����п��Ӧ����Ӧ��������Һ�е�H+��Ũ���йأ�H+��Ũ�ȹ�ϵΪ���������ᣬ���Գ�ʼ��Ӧ���ʹ�ϵΪ���������ᣬ��v2��v1��v3��
��.
��1��������Һ����ˮϡ�������Ϊԭ����10��, ���ᡢ������ǿ�������ȫ���룬����c(H��)����СΪԭ����1/10��������������ʣ���ˮϡ�ͻ��в����������ֵ��봦��������c(H��)�����С��ԭ����1/10����c(H��) �ɴ�С��˳����c��a=b��
��2��������Һ�����ͬʱ,ͬʱ������ͬ��п,��������ͬ���ʵ���������������ʱ���������ᡢ����c(H��)��ȡ�����t1=t2��������������ʣ�ֻ�в��������ӵ�����������ŷ�Ӧ�Ľ��У����������������ӡ����Դ���c(H��)������ᡢ����c(H��)�ʴ��ᷴӦ����ʱ����̡�t1=t2��t3��
���㣺����ʵĵ���
����������ע����մ���IJ��ֵ����c(H��)��Ӱ�졣

 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д���20 mL NaOH��Һ����μ���0.1 mol/L������Һ���ζ���������ͼ��ʾ�������ж���ȷ���ǣ� ��
| A����M�㣬����ǡ�÷�Ӧ��ȫ |
| B���ζ�ǰ������c(H��) ���ڼ���c(OH��) |
| C��NaOH��Һ�����ʵ���Ũ��Ϊ0.1 mol/L |
| D����N�㣬c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH) |
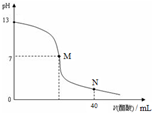 ��20mL NaOH��Һ����μ���0.1mol/L������Һ���ζ�������ͼ��ʾ�������ж���ȷ���ǣ�������
��20mL NaOH��Һ����μ���0.1mol/L������Һ���ζ�������ͼ��ʾ�������ж���ȷ���ǣ�������