题目内容
【题目】已知:还原性HSO3﹣>I﹣,氧化性IO3﹣>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.
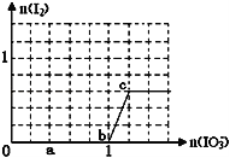
(1)a点时消耗NaHSO3的物质的量为_____mol,假设反应中无SO2逸出。
(2)从b点开始计算,当生成0.3mol I2时,转移电子数为_______个。
【答案】 1.2 0.5NA
【解析】还原性HSO-3>I-,所以首先是发生以下反应离子方程式:IO3-+3HSO3-═I-+3SO42-+3H+,继续加入KIO3,氧化性IO-3>I2,所以IO3-可以结合H+氧化I-生成I2,离子方程式是IO3-+6H++5I-═3H2O+3I2。
(1)a点碘酸钾的物质的量是0.4mol,根据碘酸钾和亚硫酸氢钠的关系式知,消耗NaHSO3的物质的量=![]() ×3=1.2mol,故答案为:1.2;
×3=1.2mol,故答案为:1.2;
(2)根据图象知,b-c段内,碘离子部分被氧化生成碘单质,发生反应的离子方程式为IO3-+6H++5I-═3H2O+3I2,反应中转移5个电子。当生成0.3mol I2时,转移电子0.5mol,数目为0.5NA,故答案为:0.5NA。

练习册系列答案
相关题目