题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 18g氨基(-ND2)中含有的电子数为10NA
B. 一定质量的乙烷与22.4L(标准状况)Cl2在光照条件下发生取代反应,形成C-Cl键的数目为2NA
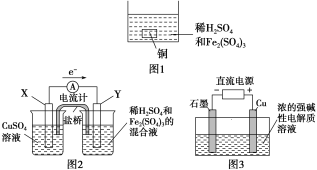
C. 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
D. n(H2SO3)和n(HSO3-)之和为1mol的KHSO3溶液中,含有的K+数目为NA
【答案】C
【解析】
A.18g该氨基的物质的量为1mol,含有的电子数为9NA,A项错误;B.若形成C-Cl键的数目为2NA,则表示氯气中所有的氯反应后均形成了C-Cl键,这显然是错误的,因为每取代一个氢原子,都还要生成一个氯化氢分子,形成H-Cl键,B项错误;C.用惰性电极电解硫酸铜溶液时,电解过程分两个阶段,第一阶段是电解硫酸铜2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,第二阶段是电解硫酸(实为电解水):2H2O
2Cu+O2↑+2H2SO4,第二阶段是电解硫酸(实为电解水):2H2O![]() 2H2↑+O2↑。阳极始终产生氧气,阴极先是产生铜,后是产生氢气,因此当阴、阳两极产生相同量的气体时,说明第一阶段和第二阶段产生的氧气的量相同,因第一阶段硫酸铜完全反应,转移电子数为0.02mol,所以两阶段共转移电子数为0.04mol,C项正确;D.KHSO3溶液中硫原子有三种存在形式:H2SO3、HSO3-和SO32-,所以该溶液中K+的数目大于1mol,D项错误;所以答案选C项。
2H2↑+O2↑。阳极始终产生氧气,阴极先是产生铜,后是产生氢气,因此当阴、阳两极产生相同量的气体时,说明第一阶段和第二阶段产生的氧气的量相同,因第一阶段硫酸铜完全反应,转移电子数为0.02mol,所以两阶段共转移电子数为0.04mol,C项正确;D.KHSO3溶液中硫原子有三种存在形式:H2SO3、HSO3-和SO32-,所以该溶液中K+的数目大于1mol,D项错误;所以答案选C项。

【题目】已知某化学反应的平衡常数表达式为K=![]() ,在不同的温度下该反应的平衡常数如表所示:下列有关叙述不正确的是( )
,在不同的温度下该反应的平衡常数如表所示:下列有关叙述不正确的是( )
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
A. 该反应的化学方程式是CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B. 上述反应的正反应是放热反应
C. 若在1 L的密闭容器中通入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO为0.4 mol,则该反应达到平衡状态
D. 若平衡浓度符合下列关系式:![]() =
=![]() ,则此时的温度为1 000 ℃
,则此时的温度为1 000 ℃