题目内容
5.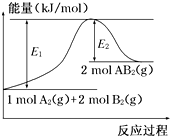 已知某化学反应A2(g)+2B2(g)═2AB2(g)(AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是( )
已知某化学反应A2(g)+2B2(g)═2AB2(g)(AB2的分子结构为B-A-B)的能量变化如图所示,下列有关叙述中正确的是( )| A. | 该反应的进行一定需要加热 | |
| B. | 该反应的△H=-(E1-E2)kJ/mol | |
| C. | 该反应中反应物的键能总和大于生成物的键能总和 | |
| D. | 断裂1 mol A-A和2 mol B-B放出E1 kJ能量 |
分析 化学反应A2(g)+2B2(g)═2AB2(g)的能量变化依据图象分析,结合反应前后能量守恒可知,反应物能量之和小于生成物的能量之和,反应是吸热反应,反应过程中断裂化学键需要吸收能量,形成化学键放出热量,据此分析.
解答 解:A、反应前后能量守恒可知,反应物能量之和小于生成物的能量之和,反应是吸热反应,吸热反应不一定都要加热,例如氢氧化钡和氯化铵在常温下就反应,故A错误;
B、该反应焓变=断裂化学键吸收热量-形成化学键所放出热量,所以焓变为△H=+(E1-E2)kJ/mol,故B错误;
C、反应是吸热反应,依据能量守恒可知,反应中反应物的总能量低于生成物的总能量,即反应物的键能总和大于生成物的键能总和,故C正确;
D、断裂化学键吸收热量,所以断裂1 mol A-A和2 mol B-B吸收E1 kJ能量,故D错误;
故选C.
点评 本题考查了反应热量变化的分析判断,图象分析,反应前后的能量守恒应用,化学键的断裂和形成与能量的关系,计算焓变的依据,题目较简单.

练习册系列答案
相关题目
5.下列说法不正确的是( )
| A. | 用食醋可除去热水壶内壁的水垢 | |
| B. | 淀粉,油脂 和蛋白质都是高分子化合物 | |
| C. | 服用铬含量超标的药用胶囊会对人对健康造成危害 | |
| D. | 新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮 |
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 水电离出的c(H+)=1.0×10-13mol/L的溶液中,Na+、NH4+、Cl-、SO42- | |
| B. | 滴入甲基橙试液变红色的溶液中:Cl-、AlO2-、HCO3-、NH4+ | |
| C. | 加入少量KSCN后变为红色的溶液中:K+、Mg2+、I-、NO3- | |
| D. | 无色透明的溶液中:CH3COO-、CO32-、K+、Na+ |
13.COCl2俗称光气,其中心C原子采用sp2杂化成键.下列对该分子结构的分子中错误的是( )
| A. | 分子中所有原子共平面 | B. | 碳氧原子之间含有1个α键和1个π键 | ||
| C. | 分子中既含单键又含双键 | D. | 分子中既含极性键又含非极性键 |
20.下列说法正确的是( )
| A. | 1 mol苯甲酸在浓H2SO4存在下与足量乙醇反应可得1 mol苯甲酸乙酯 | |
| B. | 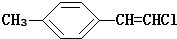 分子中的所有原子有可能共平面 分子中的所有原子有可能共平面 | |
| C. | 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有4种 | |
| D. | 1 mol阿司匹林(结构简式见图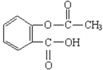 )与足量的氢氧化钠溶液加热反应,最多消耗的氢氧化钠的物质的量2 mol )与足量的氢氧化钠溶液加热反应,最多消耗的氢氧化钠的物质的量2 mol |
17.下列鉴别物质的方法不正确的是( )
| A. | 用燃烧的方法可以鉴别甲烷和乙烯 | |
| B. | 用酸性KMnO4溶液鉴别苯和CCl4 | |
| C. | 用银氨溶液鉴别蔗糖和葡萄糖 | |
| D. | 用KI溶液鉴别淀粉溶液和鸡蛋白溶液 |
14.下列离子方程式正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O | |
| C. | 草酸使高锰酸钾溶液褪色:5H2C2O4+2MnO4-+6H+═2Mn2++10 CO2↑+8H2O | |
| D. | 乙醛溶液与足量的银氨溶液共热CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$ CH3COO-+NH${\;}_{4}^{+}$+2Ag↓+3NH3+H2O |
15.发达国家一些大城市的酸雨以硝酸型为主,原因是这些城区( )
| A. | 硝酸工业发达 | B. | 雷雨天气较多 | C. | 机动车辆较多 | D. | 燃料以煤为主 |
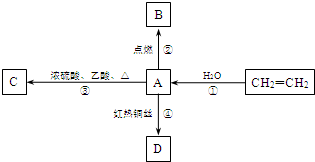 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种转化.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种转化. CH3COOCH2CH3+H2O,该反应的类型是:取代(或酯化)反应.
CH3COOCH2CH3+H2O,该反应的类型是:取代(或酯化)反应.