题目内容
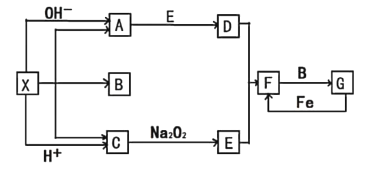
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据如图关系推断:
(1)写出化学式:A____,G____。
(2)实验室收集气体D和A的方法依次是____法、_____法。
(3)写出C→E的化学方程式:____。
(4)请写出A与E反应生成D的化学方程式:_____。
(5)检验物质A的方法和现象是______。
【答案】NH3 HNO3 排水法 向下排空气法催化剂 ![]()
![]() 用湿润的红色石蕊试纸,若遇到
用湿润的红色石蕊试纸,若遇到![]() 变蓝则说明有
变蓝则说明有![]() 存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有
存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有![]() 存在)
存在)
【解析】
根据X可以发生的离子反应判断X可能含有的离子;根据题目反应转化关系分析解答;根据化学实验基础分析解答。
X既能与OH-反应放出气体,又能与H+反应生成气体,可推断X一定含有NH4+,可能含有HCO3-或CO32-,B为H2O,X与OH-反应生成NH3,即A为NH3,C为CO2,其中CO2与Na2O2反应生成O2,即E为O2,NH3与O2反应生成NO和H2O,即D为NO,F为NO2,NO2与H2O反应生成HNO3,即G为硝酸。
(1)X能与OH-反应放出气体,即X中含有NH4+,则A为NH3,F为NO2与水反应生成HNO3,则G为硝酸;
(2)D为NO,A为NH3,由于NO密度接近空气,则不能用排空气法收集,故收集NO气体需用排水法,由于NH3极易溶于水,则收集NH3需要采用向下排空气法;
(3)C为CO2,E为O2,C→E即过氧化钠与CO2反应生成碳酸钠和氧气,化学方程式为:![]() ;
;
(4)根据分析可知,气体A为NH3,E为O2, NH3与O2反应生成NO和H2O,化学方程式: ;
;
(5)NH3是碱性气体,检验NH3可以用湿润的红色石蕊试纸,若遇到![]() 变蓝则说明有
变蓝则说明有![]() 存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有
存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有![]() 存在)。
存在)。

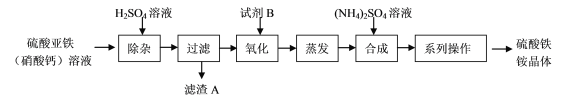
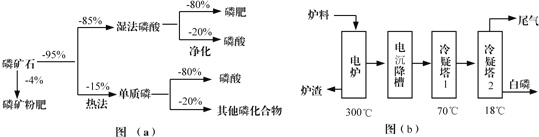
【题目】化学一选修:化学与技术磷矿石主要以[Ca3(PO4)2H2O]和磷灰石[Ca5F(PO4)3,Ca5(OH)(PO4)3]等形式存在,图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
部分物质的相关性质如下:
熔点/℃ | 沸点/℃ | 备注 | |
白磷 | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的____________;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:___________,现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸___________t。
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷,炉渣的主要成分是___________(填化学式),冷凝塔1的主要沉积物是___________,冷凝塔2的主要沉积物是___________。
(4)尾气中主要含有___________,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去___________;再通入次氯酸钠溶液,可除去___________(均填化学式)。
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是___________。