题目内容
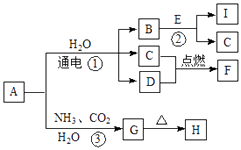
【题目】氢氧化镁是一种用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面.镁硅酸盐矿石(主要成分Mg3Si2O5(OH)4 , 含氧化铝、氧化铁、氧化亚铁等杂质)可用于生产氢氧化镁,简要工艺流程如图1: 
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是 .
(2)加入H2O2溶液反应的离子方程式是 .
(3)向溶液Ⅰ中加入的X可以是 , 作用是 .
(4)加入氨水时,Mg2+转化率随温度t的变化如图2所示: ①溶液Ⅱ中发生反应的离子方程式是 .
②t1前Mg2+转化率增大的原因是;
t1后Mg2+转化率下降的原因是(用化学方程式表示) .
【答案】
(1)改变矿石结构,提高酸浸率
(2)2Fe2++H2O2+2H+=2Fe3++2H2O
(3)MgO或Mg(OH)2、MgCO3;调节溶液pH
(4)Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+;镁离子与氨水反应是吸热反应,升高温度,平衡右移,Mg2+转化率增大;NH3?H2O ![]() ?NH3↑+H2O
?NH3↑+H2O
【解析】解:溶液Ⅰ中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子,根据题中提供的各种金属离子沉淀的pH值可知,加入双氧水可以将亚铁离子氧化成铁离子,再加入试剂X主要作用是调节溶液pH值,使铁离子沉淀,可以加氧化镁或氢氧化镁等,过滤后在滤液中加入氨水使溶液中镁离子沉淀,得氢氧化镁沉淀,由于要通过使铁离子沉淀的方法除去铁,所以要先氧化再沉淀,根据Mg2+转化率随温度t的变化示意图可知,由于氨水与镁离子反应生成氢氧化镁的反应是吸热反应,所以升高温度,镁离子的转化率增大,但随着温度的升高,氨气在水中的溶解度减小,氨水的浓度减小,会导致Mg2+转化率减小,(1)对矿石焙烧的目的是改变矿石结构,在酸浸时提高浸出率,减少所需物质的损失,所以答案是:改变矿石结构,提高酸浸率;(2)根据上面的分析可知,要先氧化再沉淀,所以向溶液Ⅰ中加入H2O2是为了将二价铁氧化为三价铁,离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,所以答案是:2Fe2++H2O2+2H+=2Fe3++2H2O;(3)根据上面的分析可知,向溶液Ⅰ中加入X的作用是调节溶液pH是三价铁离子沉淀,加入的物质不能引入新杂质,可加入MgO或Mg(OH)2、MgCO3 , 与三价铁水解生成的氢离子反应,使平衡向生成沉淀的方向移动,
所以答案是:MgO或Mg(OH)2、MgCO3;调节溶液pH;(4)①向溶液Ⅱ中加入氨水与镁离子反应生成氢氧化镁沉淀,反应的离子方程式是 Mg2++2NH3H2O=Mg(OH)2↓+2NH4+ ,
所以答案是:Mg2++2NH3H2O=Mg(OH)2↓+2NH4+;②根据上面的分析可知,t1前Mg2+转化率增大的原因是 升高温度,Mg2+转化率增大,平衡右移,反应是吸热反应;t1后Mg2+转化率下降的原因是氨气在水中的溶解度减小,氨水的浓度减小,反应的方程式为 NH3H2O ![]() NH3↑+H2O,
NH3↑+H2O,
所以答案是:镁离子与氨水反应是吸热反应,升高温度,平衡右移,Mg2+转化率增大;NH3H2O ![]() NH3↑+H2O.
NH3↑+H2O.