题目内容
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高正价和最低负价之和为0;Z的非金属性在同周期元素中最强。下列说法正确的是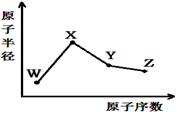
| A.对应气态氢化物的稳定性:Y>Z |
| B.化合物XZW既含离子键也含共价键 |
| C.对应简单离子半径:W>X |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
BC
解析试题分析:由题意可知W的质子数是8,所以W是O元素;X、Y、Z属于第三周期元素,X的原子半径最大,所以X是Na元素;Y的最高正价和最低负价之和为0,所以Y是Si元素;Z的非金属性在同周期元素中最强,则Z 是Cl元素。A、Z的非金属性比Y强,所以对应气态氢化物的稳定性:Y<Z,错误;B、NaClO中既含离子键也含共价键,周期;C、W与X的离子的核外电子层结构相同,所以核电荷数小的离子半径大,W>X,周期;D、二氧化硅与氢氧化钠溶液反应,但不与高氯酸溶液反应,错误,答案选BC。
考点:考查元素推断,元素周期律的应用,物质性质判断

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案Se是人体必需微量元素,下列有关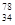 Se和
Se和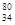 Se的说法正确的是
Se的说法正确的是
A.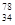 Se 和 Se 和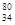 Se所含电子数不同 Se所含电子数不同 | B.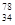 Se和 Se和 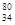 Se是两种不同的核素 Se是两种不同的核素 |
C.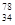 Se和 Se和 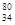 Se 分别含有44和46个质子 Se 分别含有44和46个质子 | D.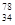 Se和 Se和 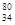 Se都含有34个中子 Se都含有34个中子 |
下列说法不正确的是( )
①质子数相同的粒子一定是同一种元素
②质子数相同且电子数也相同的两种粒子不可能一种是分子,另一种是离子
③电子数相同的粒子不一定是同种元素
④一种元素不可以形成不同的单质
⑤某元素的相对原子质量取整数值就是质量数
| A.②④⑤ | B.①④⑤ | C.②③④ | D.①②③④⑤ |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍。下列说法中不正确的是
| A.W、M的某种单质可作为水处理中的消毒剂 |
| B.电解YW2的熔融物可制得Y和W的单质 |
| C.相同条件下,W的氢化物水溶液酸性比Z弱 |
| D.X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
已知X、Y、Z、W四种短周期主族元素在周期表中相对位置如图所示,下列说法不正确的是
| X | Y |
| Z | W |
A.Y原子形成的简单离子半径一定比X原子形成的简单离子半径小
B.W的原子序数可能是Y的原子序数的3倍
C.W的气态氢化物的稳定性一定比Y的强
D.若Z元素最高价氧化物的水化物是强酸,则W元素的单质具有强氧化性
O、W、X、Y、Z五种短周期元素在元素周期表中的相对位置如图所示,W是大气中含量最高的元素,由此可知 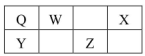
A.Q的一种核素中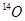 的质子数和中子数相等 的质子数和中子数相等 |
| B.X的最高正化合价与最低负化合价的绝对值之差为6 |
| C.Y是常见的半导体材料 |
| D.Z的氧化物的水化物是强酸 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.微粒X2-与Y2+核外电子排布相同,离子半径:X2-> Y2+ |
| B.人们可在周期表的过渡元素中寻找催化剂、耐腐蚀和耐高温的合金材料 |
| C.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F |
| D.Be元素与Al元素同处在周期表的金属与非金属的交界处,可推出: |
与氢氧根具有相同的质子数和电子数的微粒是
| A.CH4 | B.NH4+ | C.NH2- | D.Cl- |
右表为元素周期表前四周期的一部分,下列有关W、X、Y、Z、R五种元素的叙述中,正确的是( )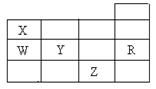
| A.常温下,Z单质为气态物质 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的稳定性要比X的氢化物的稳定性强 |
| D.Y元素的非金属性比W元素的非金属性强 |