题目内容
【题目】铬是一种银白色的金属,常用于金属加工、电镀等。工业以铬铁矿[主要成分是Fe(CrO2)2]为原料冶炼铬及获得强氧化剂Na2Cr2O7。其工艺流程如图所示:
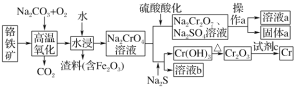
已知:高温氧化时发生反应Fe(CrO2)2+Na2CO3+O2→Na2CrO4+Fe2O3+CO2(未配平)
回答下列问题:
(1)将铬铁矿的主要成分Fe(CrO2)2写成氧化物的形式:__,高温氧化时可以提高反应速率的方法为___(写出一条即可)。
(2)Na2CrO4加入硫酸酸化的离子方程式为__;在实验室中,操作a所用到的玻璃仪器有__。
(3)Na2CrO4中铬元素化合价为__;生成1molNa2CrO4时共转移电子的物质的量为__mol。
(4)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol·L-1以下才能排放,可采用加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入硫酸处理多余的Ba2+的方法处理废水,加入可溶性钡盐后,废水中Ba2+的浓度应大于__mol·L-1,废水处理后达到国家标准才能排放。
【答案】FeO·Cr2O3 将固体磨碎或不断搅拌 2CrO42-+2H+=Cr2O72-+H2O 烧杯、漏斗、玻璃棒 +6 3.5 2.4×10-4
【解析】
铬铁矿[主要成分是Fe(CrO2)2]中加入碳酸钠并通入氧气,高温下将Fe(CrO2)2氧化得到Fe2O3、Na2CrO4,同时生成CO2,将得到的固体溶于水得到Na2CrO4溶液。向一份Na2CrO4溶液中加入硫酸酸化,硫酸和Na2CrO4反应生成Na2Cr2O7和硫酸钠,通过蒸发浓缩、冷却结晶,过滤得到固体a和溶液a;另一份Na2CrO4溶液中加入Na2S发生氧化还原反应,铬元素转化为Cr(OH)3沉淀,过滤后灼烧Cr(OH)3得到Cr2O3,可以利用热还原法制备金属铬;据此分析解答。
(1)Fe(CrO2)2 中铁元素化合价是+2价,氧化物为FeO,铬元素化合价+3价,氧化物为Cr2O3,所以Fe(CrO2)2写成氧化物形式为FeOCr2O3;增大反应物的接触面积可以加快反应速率,升高温度可以加快反应速率,不断搅拌,使固体混合物充分混合也可以加快反应速率,故答案为:FeOCr2O3 ;将固体磨碎或不断搅拌等;
(2)Na2CrO4加入硫酸酸化反应生成重铬酸钠,反应的离子方程式为2CrO42-+2H+=Cr2O72-+H2O;操作a为过滤,所用到的玻璃仪器有烧杯、漏斗、玻璃棒,故答案为:2CrO42-+2H+=Cr2O72-+H2O;烧杯、漏斗、玻璃棒;
(3)Na2CrO4中Na元素为+1价,O为-2价,则铬元素化合价为+6价;根据Fe(CrO2)2+Na2CO3+O2→Na2CrO4+Fe2O3+CO2,反应中铬元素由+3价升高为+6价,铁元素由+2价升高为+3价,1mol Fe(CrO2)2被氧化转移7mol电子,因此生成1molNa2CrO4时转移3.5mol电子,故答案为:+6;3.5;
(4)CrO42-+Ba2+BaCrO4,根据题意CrO42-的浓度降至5.0×10-7mol·L-1以下才能排放,则Ksp(BaCrO4)=c(CrO42-)×c(Ba2+)=5.0×10-7×c(Ba2+)=1.2×10-10,解得:c(Ba2+)=2.4×10-4mol/L,即Ba2+的浓度应大于2.4×10-4mol/L,故答案为:2.4×10-4。

【题目】“飘尘”是物质燃烧时产生的粒子漂浮物,颗粒很小(直径小于10-7m),不易沉降(可漂浮数小时甚至数年),它与空气中SO2、O2接触时,SO2部分转化为SO3,使空气中酸度增加形成酸雨。
(1)下列关于SO2的叙述中,正确的是_____;
A.SO2既可以做氧化剂,也可以做还原剂 B.SO2不是大汽污染物 C.大气中SO2的主要来源是汽车排出的尾气 D.SO2具有漂白性,因而可以使石蕊溶液褪色
(2)下列反应中,SO2表现了还原性的是_______;
A.SO2+H2OH2SO3 B.SO2+2NaOH=Na2CO3+H2O C.2SO2+O2![]() 2SO3 D.SO2+CaO=CaSO3
2SO3 D.SO2+CaO=CaSO3
(3)不能鉴别二氧化碳和二氧化硫的试剂是________;
A.品红溶液 B.澄清石灰水 C.溴水 D.酸性高锰酸钾溶液
(4)下列哪种危害不是酸雨导致的_______;
A.造成洪涝灾害 B.腐蚀建筑物 C.恶化人类环境 D.导致树木枯萎
(5)根据SO2通入不同溶液中实验现象,所得结论不正确的是_______;
溶液 | 现象 | 结论 | |
A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
(6)减少酸雨产生的途径可采取下列的哪些措施___________。
①少用煤做燃料 ②把工厂烟囱造高 ③燃料脱硫 ④飞机、汽车等交通工具采用清洁燃料,如天然气等 ⑤开发新能源
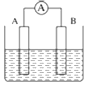
【题目】由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是( )
装置 |
|
|
|
现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
A.装置甲中X作原电池正极
B.装置乙中Y电极上的反应式为Cu2++2e=Cu
C.装置丙中溶液的c(H+)不变
D.四种金属的活动性强弱顺序为Z>W>X>Y