题目内容
【题目】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1) SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式___________。
(2) SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g) ΔH1=+48 kJ·mol-1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) ΔH2=-30 kJ·mol-1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的ΔH为____kJ·mol-1。
(3)对于反应2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
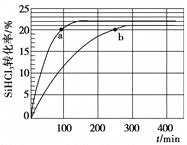
①343 K时,反应的平衡转化率α=________%。平衡常数K343 K=________(保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是______;要缩短反应达到平衡的时间,可采取的措施有_________。
(4)甲醇水蒸气重整制氢(SRM)系统简单,产物中H2 含量高、CO含量低(CO会损坏燃料电池的交换膜),是电动汽车氢氧燃料电池理想的氢源。反应如下:
反应I(主) :CH3OH(g)+ H2O(g) ![]() CO2(g)+ 3H2(g) ΔH1=+49kJ/mol
CO2(g)+ 3H2(g) ΔH1=+49kJ/mol
反应II(副) :H2(g)+ CO2(g) ![]() CO(g)+ H2O(g) ΔH2=+41kJ/mol
CO(g)+ H2O(g) ΔH2=+41kJ/mol
温度高于300℃则会同时发生反应III: CH3OH(g) ![]() CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
反应1能够自发进行的原因是_________,升温有利于提高CH3OH转化率,但也存在一个明显的缺点是________。写出一条能提高CH3OH转化率而降低CO生成率的措施_______。
【答案】2SiHCl3+3H2O=(HSiO)2O+6HCl +114 22 0.02 移走生成物 加入催化剂 该反应为熵增大的反应 升温会促进反应III的发生,提高CO的含量,而CO会破坏该电池的交换膜 加入水蒸气或使用更合适的催化剂
【解析】
(1)SiHCl3遇潮气时发烟生成(HSiO)2O等,说明反应物为SiHCl3、H2O,生成物为(HSiO)2O、HCl,从而写出该反应的化学方程式。
(2)利用盖斯定律进行计算。
(3)假设起始量,再从坐标图象中提取转化率数据,采用三段式进行相关计算。
(4)利用自由能方程分析反应自发进行的原因,再利用题给信息找出升温的缺陷,并找到提高转化率减少CO生成量的措施。
(1)该反应的化学方程式2SiHCl3+3H2O=(HSiO)2O+6HCl;
答案:2SiHCl3+3H2O=(HSiO)2O+6HCl。
(2) 2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g) ΔH1=+48 kJ·mol-1 ①
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) ΔH2=-30 kJ·mol-1 ②
将①×3+②得:4SiHCl3(g)=SiH4(g)+3SiCl4(g) ΔH=+114kJ·mol-1;
答案:+114。
(3)因为温度越高,反应速率越快,达平衡的时间越短,所以a为343 K时SiHCl3的转化率曲线,b为323 K时SiHCl3的转化率曲线。
①从图中可以看出,343 K时,反应的平衡转化率α=22%,
设反应物的起始浓度为2mol/L
2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)
SiH2Cl2(g)+SiCl4(g)
起始量 2mol/L 0 0
变化量 0.44mol/L 0.22mol/L 0.22mol/L
平衡量 1.56mol/L 0.22mol/L 0.22mol/L
平衡常数K343 K=![]() ;
;
答案为:22%;0.02。
②在343 K下,要提高SiHCl3转化率,可采取的措施是移走生成物;
要缩短反应达到平衡的时间,可采取的措施有加入催化剂,加快反应速率;
答案为:移走生成物;加入催化剂。
(4)依据自由能方程,G=H-TS,H>0,要使G<0,S>0。反应1能够自发进行的原因是该反应为熵增大的反应;
从题给信息可以看出,升温有利于反应I,有利于反应II,还会促进反应III的发生。即提高CH3OH转化率,但也存在一个明显的缺点是升温会促进反应III的发生,提高CO的含量,而CO会破坏该电池的交换膜。
水蒸气为主反应的反应物,故加入水蒸气可以提高甲醇的转化率,同时使反应II的平衡逆向移动,从而降低了CO的生成率;也可使用更合适的催化剂,最好只催化反应I,不催化反应II,也能达到目的。
所以能提高CH3OH转化率而降低CO生成率的措施为加入水蒸气或加入更合适的催化剂。
答案为:该反应为熵增大的反应;升温会促进反应III的发生,提高CO的含量,而CO会破坏该电池的交换膜;加入水蒸气或使用更合适的催化剂。