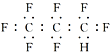��Ŀ����
����Ŀ��ijУѧ��Ϊ̽�������巢����Ӧ��ԭ��������ͼװ�ý���ʵ�飮
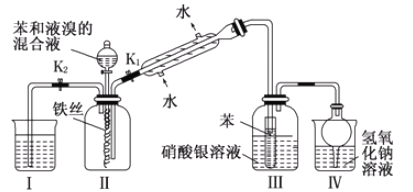
�������֪ʶ�ش��������⣺
��1��ʵ�鿪ʼʱ���ر�K1������K2�ͷ�Һ©���������μӱ���Һ��Ļ��Һ����Ӧ��ʼ����Ӧ�Ļ�ѧ����ʽ_____����һ������ڣ�����ƿ�۲쵽_____�����п��ܹ۲쵽��������____
��2������ʵ��װ�����ܷ�ֹ������װ����_____����װ����ţ���
��3����Ӧ������Ҫʹװ�ã�I���е�ˮ������װ�ã����У�����������Ŀ����______
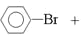
���𰸡�![]() +Br2
+Br2![]()
 HBr ��ɫ��״Һ�壨�屽�� �а������֣����ƿ����Һ����dz��ɫ�廯���������� III��IV ��ȥ�廯�����壬�����ݳ���Ⱦ����
HBr ��ɫ��״Һ�壨�屽�� �а������֣����ƿ����Һ����dz��ɫ�廯���������� III��IV ��ȥ�廯�����壬�����ݳ���Ⱦ����
��������
��1������Һ�������������������·���ȡ����Ӧ�����屽���廯�⣻�ڣ����������屽���������廯������������Һ��Ӧ�����廯����
��2�����е��ܿ��ڱ���Һ�����ϣ�����ܿɷ�������
��3�������廯��������ˮ������
��1������Һ�������������������·���ȡ����Ӧ�����屽���廯�⣬��Ӧ����ʽ��![]() +Br2
+Br2![]()
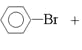 HBr���ڣ����������屽���������к�ɫ��״Һ�壻�������廯������������Һ��Ӧ�����廯�����������а������֣����ƿ����Һ����dz��ɫ�廯���������ɣ�
HBr���ڣ����������屽���������к�ɫ��״Һ�壻�������廯������������Һ��Ӧ�����廯�����������а������֣����ƿ����Һ����dz��ɫ�廯���������ɣ�
��2�����е��ܿ��ڱ���Һ�����Ͽɷ����������������ϴ�ɷ�����������ʵ��װ�����ܷ�ֹ������װ���Т��IV��
��3���廯��������ˮ����Ӧ������Ҫʹװ�ã�I���е�ˮ������װ�ã����У����Գ�ȥ�廯�����壬�����ݳ���Ⱦ������

 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д� â���̸����������������ϵ�д�
â���̸����������������ϵ�д�����Ŀ��A���֣����Ӣɰ(ZrO2��SiO2����������Fe2O3��Al2O3��SiO2������)�Ʊ�ZrO2���������£�

��֪����ZrO2��ǿ������Һ����ZrO32-��ʽ���ڣ���ǿ������Һ����ZrO2+��ʽ���ڡ�
�ڲ��ֽ���������ʵ�������¿�ʼ��������ȫ������pH���±���
Mn+ | Fe3+ | Al3+ | ZrO2+ |
��ʼ����ʱpH | 1.9 | 3.3 | 6.2 |
������ȫʱpH | 3.8 | 5.6 | 8.0 |
(1)����I����Ҫ�IJ�������Ϊ___________������I���˵õ���Һa���ɵõ�_________��
(2)�Ӱ�ˮ����Һa�е���pH�ĵķ�Χ��________________��
(3)����II��õ���Һb������II������II����������£�
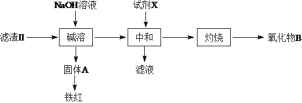
������B�Ļ�ѧʽΪ__________�����Լ�XΪ���ᣬȱ����___________��
(4)����III���õ�Zr(OH)4��õ�ij����Һ�������Һ�м���CaCO3��ĩ�����ȣ��õ��������塣�÷�Ӧ�����ӷ���ʽΪ_____________________________��
(5)���백ˮ����Һb���������ӷ���ʽΪ__________________________��
(6)Ϊ�õ�������ZrO2��Zr(OH)4��Ҫϴ�ӣ�����Zr(OH)4�Ƿ�ϴ�Ӹɾ��ķ�����______________��
B���֣��Ѿ����Ǵ���������Ѵ������в�ѡ��������Ҫ�ɷ�ΪFeTiO3����������;�dz��㷺���Ѱ۵�ԭ�ϡ����Ѿ���ʯΪԭ���Ʊ������ѵ���������ͼ��ʾ(ijЩ���˹����Ѻ���)����֪ǿ������Һ�У�+4�۵���Ԫ����TiO2+��ʽ���ڣ������Ѳ�����ϡ���������ᡣ�ش��������⣺

(1)�����������������__________________��
(2)����K�׳��̷�������K�Ļ�ѧʽΪ____________��
(3)��д����ҺC�����Ʊ���������Ļ�ѧ����ʽ__________________________________��
(4)�����������Ļ���̿�������Ļ�ѧ����ʽΪ_______________����֪TiO2+2Cl2![]() TiCl4+O2Ϊ���ȷ�Ӧ���Ҹ������·�ӦҲ�ܹ�������Ϊ���Ʊ�TiCl4�����л�Ҫ�������̿���Խ���ԭ��_________________��
TiCl4+O2Ϊ���ȷ�Ӧ���Ҹ������·�ӦҲ�ܹ�������Ϊ���Ʊ�TiCl4�����л�Ҫ�������̿���Խ���ԭ��_________________��
(5)����F�����F��������_____________________��
(6)��ҺH��_________������Ϊ___________________________��