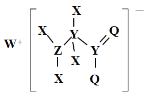题目内容
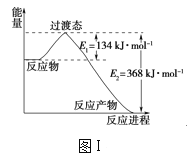
【题目】(1)图Ⅰ是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,请写出NO2和CO反应的热化学方程式:__。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=49.0kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
又知:③H2O(g)=H2O(l) ΔH=-44kJ·mol-1
则甲醇蒸气完全燃烧生成液态水的热化学方程式为__。
(3)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ·mol-1) | a | b | c | x |
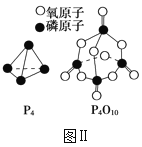
已知1molP4(g)完全燃烧生成P4O10(g)放出的热量为dkJ,P4和P4O10的结构如图Ⅱ所示,则上表中x=___(用含有a、b、c、d的代数式表示)。
【答案】NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234kJ·mol-1 CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=-764.7kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-764.7kJ·mol-1 ![]() (d+6a+5c-12b)
(d+6a+5c-12b)
【解析】
(1)根据图示中能量变化及热化学方程式书写原则进行书写;(2)依据热化学方程式,利用盖斯定律进行计算;(3)白磷燃烧的方程式为P4+5O2=P4O10,根据化学键的断裂和形成的数目进行计算。
(1)由图可知,1molNO2和1molCO反应生成CO2和NO放出热量为:368 kJ 134 kJ =234kJ,则反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g) △H=-234kJ·mol-1,故答案为:NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234kJ·mol-1;
(2)利用盖斯定律进行计算,
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=49.0kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44kJ·mol-1
依据盖斯定律计算②×3①×2+③×2得到CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=(-192.9kJ·mol-1)×3-(49.0kJ·mol-1×2)+(-44kJ·mol-1)×2=-764.7kJ·mol-1;故答案为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l) ΔH=(-192.9kJ·mol-1)×3-(49.0kJ·mol-1×2)+(-44kJ·mol-1)×2=-764.7kJ·mol-1;故答案为:CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=-764.7kJ·mol-1;
O2(g)=CO2(g)+2H2O(l) ΔH=-764.7kJ·mol-1;
(3)白磷燃烧的方程式为P4+5O2=P4O10,1mol白磷完全燃烧需拆开6molPP、5molO=O,形成12molPO、4molP=O,所以(6mol×akJ/mol+5mol×ckJ/mol)12mol×bkJ/mol+4mol×xkJ/mol=dkJ/mol,x=![]() (d+6a+5c-12b)kJ/mol,故答案为:
(d+6a+5c-12b)kJ/mol,故答案为:![]() (d+6a+5c-12b)。
(d+6a+5c-12b)。