题目内容
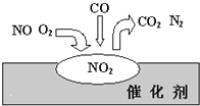
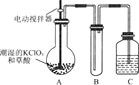
【题目】二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KC1O3和草酸(H2C2O4)在60℃时反应制得。某学生用下图所示的装置模拟工业制取及收集C1O2,其中A为C1O2的发生装置,B为C1O2的凝集装置,C为尾气吸收装置。
请回答下列问题:
(1)A中反应产物有K2CO3、C1O2和CO2等,请写出该反应的化学方程式:________________________。
A部分还应添加温水浴控制温度在60 °C,B部分还应补充什么装置:_________________。
(2)该装置按(1)补充完整后,装置A、B、C中还有一处设计明显不合理的是_____(填“A”“B”或“C”)。
(3)C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),该反应的离子方程式为____________。若实验时需要450 mL 4 mol L-1的NaOH溶液,则在精确配制时,需要称取NaOH的质量是____g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有_______。
【答案】 2KClO3+H2C2O4=K2CO3+2ClO2↑+CO2↑+ H2O 盛有冰水混合物的水槽(或冰水浴) C 2ClO2+2OH-==ClO3-+ClO2-+ H2O 80.0 500 mL容量瓶、烧杯
【解析】(1)A中反应产物有K2CO3、ClO2、CO2,由反应物与生成物可知反应为2KClO3+H2C2O4=K2CO3+2ClO2↑+CO2↑+H2O,因为B为ClO2的凝集装置,又二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,所以B部分还应补充装置为冰水浴冷凝装置或盛有冰水的水槽,故答案为:2KClO3+H2C2O4=K2CO3+2ClO2↑+CO2↑+H2O;冰水浴冷凝装置或盛有冰水的水槽;
(2)C处为密封装置,过量气体不能排出,可导致仪器炸裂,则C不合理,故答案为:C;
(3)C为尾气吸收装置,可选择NaOH溶液来吸收尾气,发生的氧化还原反应为2ClO2+2NaOH═NaClO2+NaClO3+H2O,离子反应为2ClO2+2OH-=ClO2-+ClO3-+H2O,配制450mL4mol/L的NaOH溶液,应该选用500mL容量瓶、根据提供的仪器可知,还需要烧杯,需要NaOH的质量为0.5L×4mol/L×40g/mol=80.0g,故答案为:2ClO2+2OH-=ClO2-+ClO3-+H2O;80.0;500mL容量瓶、烧杯。

【题目】用下图装置可以完成一系列实验(图中夹持装置及加热装置已略去),不考虑①②③中物质间的相互影响。请回答下列问题:
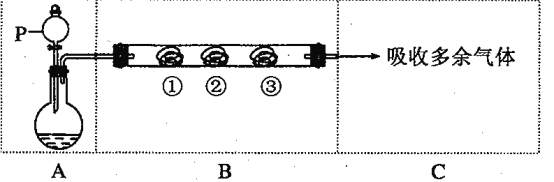
(1)若装置A选用浓盐酸和二氧化锰混合制取Cl2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
B中棉花的位置 | ① | ② | ③ |
所蘸试剂 | 石蕊溶液 | 淀粉KI溶液 | 浓氨水 |
现象 | ________ | ________ | ________ |
涉及的化学方程式 | ________ | ________ | 3Cl2+8NH3=6NH4Cl+N2 |
(2)若装置A选用浓硫酸和亚硫酸钠固体制取SO2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
B中棉花的位置 | ① | ② | ③ |
所蘸试剂 | H2S溶液 | 酸性KMnO4溶液 | 品红溶液 |
现象 | ________ | ________ | 褪色 |
体现SO2的性质 | ________ | ________ | ________ |