题目内容
(12分)有A、B、C、D、E、F六种元素,已知:
①.它们位于三个不同短周期,核电荷数依次增大.
②.E元素的电离能数据见下表(kJ·mol-1):
③.B与F分别同主族.
④.A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物.
⑤.B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物.
⑴写出A、B、C、D、E、F元素符号分别为___________________________________,
只含有A、B、D、E四种元素的两种无水盐的化学式 _____ ._____________.
(2)B2A2分子结构式______________中存在____个σ键,_____个兀键.
(3)下列四种物质形成的晶体,熔点由高到低的顺序(用a、b、c 、d表示): .
a.F与B形成的化合物 b.B与D形成的稳定化合物
c.F的单质 d. E与D形成的化合物
①.它们位于三个不同短周期,核电荷数依次增大.
②.E元素的电离能数据见下表(kJ·mol-1):
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
④.A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物.
⑤.B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物.
⑴写出A、B、C、D、E、F元素符号分别为___________________________________,
只含有A、B、D、E四种元素的两种无水盐的化学式 _____ ._____________.
(2)B2A2分子结构式______________中存在____个σ键,_____个兀键.
(3)下列四种物质形成的晶体,熔点由高到低的顺序(用a、b、c 、d表示): .
a.F与B形成的化合物 b.B与D形成的稳定化合物
c.F的单质 d. E与D形成的化合物
⑴. H C N O Na Si (3分) NaHCO3 CH3COONa (或其它有机酸的盐)
(2). H-C≡C-H 3 , 2 (3).a c d b
(2). H-C≡C-H 3 , 2 (3).a c d b
(1)根据E的电离能数据可知,E应该是第IA元素。所以根据元素的结构、位置、性质可知A、B、C、D、E、F六种元素分别是H C N O Na Si 。只含有A、B、D、E四种元素的两种无水盐的化学式分别是NaHCO3、CH3COONa(或甲酸钠等)。
(2)乙炔分子中含有碳碳三键,其结构式为H-C≡C-H 。单键都是σ键,而三键都是由1个σ键和2个兀键构成的,所以乙炔分子中含有3个σ键,2个兀键。
(3)a是SiC属于原子晶体,b是CO2属于分子晶体,c是硅,也属于原子晶体,但硅原子半径大于碳原子的,属于熔点小于SiC的,d是氧化钠,属于离子晶体,所以熔点由高到低的顺序是a c d b 。
(2)乙炔分子中含有碳碳三键,其结构式为H-C≡C-H 。单键都是σ键,而三键都是由1个σ键和2个兀键构成的,所以乙炔分子中含有3个σ键,2个兀键。
(3)a是SiC属于原子晶体,b是CO2属于分子晶体,c是硅,也属于原子晶体,但硅原子半径大于碳原子的,属于熔点小于SiC的,d是氧化钠,属于离子晶体,所以熔点由高到低的顺序是a c d b 。

练习册系列答案
相关题目
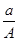 (A-N+m)mol
(A-N+m)mol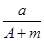 (A-N)mol
(A-N)mol