题目内容
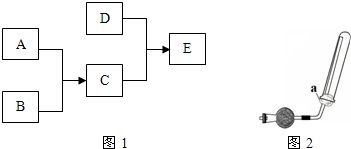
A、B、C、D、E五种短周期元素的原子序数依次增大,且知:
(1)其原子半径大小关系是:D>E>B>C>A。
(2)A、D同主族,并可形成离子晶体DA、
(3)B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素。
(4)B、E两种元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和。
请填写下列空白:
(1)DA与水反应后所得溶液的pH_________(填“>”“<”或“=”)7。
(2)D2C2的电子式__________________。
(3)1 mol E单质与足量的D的最高价氧化物的水化物溶液反应,能产生_________mol A2气体,并写出其反应的离子方程式__________________。
(4)写出B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水的离子方程式:
_____________________________________________________。
_____________________________________________________。
_____________________________________________________。
_____________________________________________________。
(5)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为___________________________。
(1)其原子半径大小关系是:D>E>B>C>A。
(2)A、D同主族,并可形成离子晶体DA、
(3)B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素。
(4)B、E两种元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和。
请填写下列空白:
(1)DA与水反应后所得溶液的pH_________(填“>”“<”或“=”)7。
(2)D2C2的电子式__________________。
(3)1 mol E单质与足量的D的最高价氧化物的水化物溶液反应,能产生_________mol A2气体,并写出其反应的离子方程式__________________。
(4)写出B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水的离子方程式:
_____________________________________________________。
_____________________________________________________。
_____________________________________________________。
_____________________________________________________。
(5)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为___________________________。
(1)>
(2)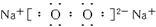
(3)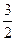 2Al+2OH-+2H2O====2
2Al+2OH-+2H2O====2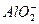 +3H2↑
+3H2↑
(4)H++OH-====H2O
Al(OH)3+3H+====Al3++3H2O
Al(OH)3+OH-====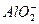 +2H2O
+2H2O
(5)4NH3+6NO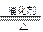 5N2+6H2O
5N2+6H2O
(2)
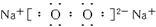
(3)
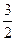 2Al+2OH-+2H2O====2
2Al+2OH-+2H2O====2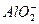 +3H2↑
+3H2↑(4)H++OH-====H2O
Al(OH)3+3H+====Al3++3H2O
Al(OH)3+OH-====
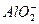 +2H2O
+2H2O(5)4NH3+6NO
 5N2+6H2O
5N2+6H2O本题考查元素及其化合物的有关性质,考查知识的综合运用能力。由题意A、D同主族,A的原子序数及原子半径最小,D的原子半径最大,可知:A为H,D为Na;所得的盐中均含有C元素,可知C元素为氧元素;由(4)可知B为N, E为Al。NaH与水反应生成NaOH和H2,溶液显碱性。Na2O2是含有过氧键的离子化合物,HNO3、NaOH、Al(OH)3三者之间两两反应,体现了酸碱中和和Al(OH)3的两性。NH3和NO催化反应生成N2和水。

练习册系列答案
相关题目

 C:____________;
C:____________;