题目内容
13. 乙基香兰素是一种合成香料,其结构简式如图:
乙基香兰素是一种合成香料,其结构简式如图:(1)以下推测正确的是d(填字母).
a.从分子结构上看,它属于芳香烃
b.该物质能与FeCI2发生显色反应
c.该物质能与碳酸钠溶液反应产生CO2气体
d.一定条件下,1mol该物质最多能与4mol H2发生加成反应
(2)R物质属于乙基香兰素的同分异构体,其性质如下:
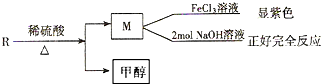
试写出任意一种符合上述条件的R的同分异构体的结构简式(任写两种):
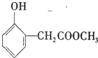 、
、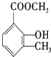 ;
;(3)X也是乙基香兰素的同分异构体,其可以发生如下反应.
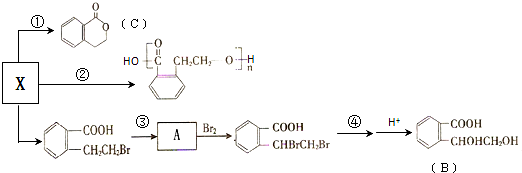
(Ⅰ)X的结构简式
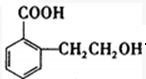 ;B中含氧官能团的名称羟基、羧基;
;B中含氧官能团的名称羟基、羧基;(Ⅱ)反应①的反应类型酯化反应或取代反应;化合物C的分子式C9H8O2;
(Ⅲ)反应④的试剂是NaOH的水溶液;反应④的化学方程式为
 .
.
分析 (1)a.烃中只含C、H元素;
b.酚羟基能和FeCl3发生显色反应但不和FeCl2发生显色反应;
c.酚羟基能和碳酸钠反应生成酚钠和碳酸氢钠;
d.苯环和碳氧双键都能发生加成反应;
(2)R水解生成甲醇和M,M能和氯化铁溶液发生显色反应,则M中含有酚羟基,M能和2mol氢氧化钠恰好反应,结合R的分子式知,M中还含有羧基,lmol R与溴水发生取代反应时,消耗1mol溴,说明R酚羟基的邻位或对位有取代基,据此推断R的结构简式;
(3)X能发生反应生成缩聚反应生成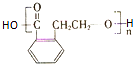 ,则X的结构简式为:
,则X的结构简式为: ,X发生分子内酯化反应生成
,X发生分子内酯化反应生成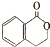 ,X发生取代反应生成
,X发生取代反应生成 ,
, 发生反应生成A,A和溴反应生成
发生反应生成A,A和溴反应生成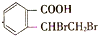 ,则A中含有碳碳双键,其结构简式为
,则A中含有碳碳双键,其结构简式为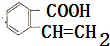 ,
,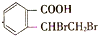 和氢氧化钠的水溶液发生取代反应然后酸化生成
和氢氧化钠的水溶液发生取代反应然后酸化生成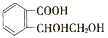 .
.
解答 解:(1)a.该分子中还含有O元素,所以不属于烃,故错误;
b.酚羟基能和FeCl3发生显色反应但不和FeCl2发生显色反应,故错误;
c.醛基能被酸性高锰酸钾氧化生成羧基,酚羟基能和碳酸钠反应生成酚钠和碳酸氢钠,所以没有二氧化碳生成,故错误;
d.苯环和碳氧双键都能发生加成反应,所以1mol该物质最多能与4molH2发生加成反应,故正确;
故选 d;
(2)R水解生成甲醇和M,M能和氯化铁溶液发生显色反应,则M中含有酚羟基,M能和2mol氢氧化钠恰好反应,结合R的分子式知,M中还含有羧基,lmol R与溴水发生取代反应时,消耗1mol溴,说明R酚羟基的邻位或有取代基,则符合条件的R的结构简式为: 、
、 ,
,
故答案为: ;
; ;
;
(3)X能发生反应生成缩聚反应生成 ,则X的结构简式为:
,则X的结构简式为: ,X发生分子内酯化反应生成
,X发生分子内酯化反应生成 ,X发生取代反应生成
,X发生取代反应生成 ,
, 发生反应生成A,A和溴反应生成
发生反应生成A,A和溴反应生成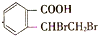 ,则A中含有碳碳双键,其结构简式为
,则A中含有碳碳双键,其结构简式为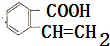 ,
,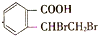 和氢氧化钠的水溶液发生取代反应然后酸化生成
和氢氧化钠的水溶液发生取代反应然后酸化生成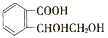 .
.
(Ⅰ)根据上面的分析可知,X的结构简式为: ,根据B的结构简式可知,B中含氧官能团的名称为羟基、羧基,
,根据B的结构简式可知,B中含氧官能团的名称为羟基、羧基,
故答案为: ;羟基、羧基;
;羟基、羧基;
(Ⅱ)反应①的反应类型是酯化反应或取代反应,根据C的结构简式可知,化合物C的分子式为C9H8O2,
故答案为:酯化反应或取代反应;C9H8O2;
(Ⅲ)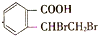 和氢氧化钠的水溶液发生取代反应然后酸化生成
和氢氧化钠的水溶液发生取代反应然后酸化生成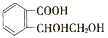 ,反应方程式为:
,反应方程式为: ,
,
故答案为: .
.
点评 本题考查了有机物的推断,明确有机物的官能团及其性质是解本题关键,结合反应条件来分析解答,注意酚羟基能和碳酸钠溶液反应,但不生成二氧化碳,为易错点.

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案| A. | 原子序数:d>c>b>a | B. | 原子半径:r (A)>r (B)>r (D)>r (C) | ||
| C. | 单质的还原性:A>B>D>C | D. | 离子半径:r (C3-)>r (D-)>r (B+)>r (A2+) |
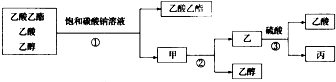 如图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图,实验过程中,所涉及的三次分离操作分别是( )
如图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图,实验过程中,所涉及的三次分离操作分别是( )| A. | ①蒸馏 ②过滤 ③分液 | B. | ①分液 ②蒸馏 ③过滤 | ||
| C. | ①蒸馏 ②分液 ③分液 | D. | ①分液 ②蒸馏 ③蒸馏 |
| Z | |
| X | Y |
| A. | Z元素的最高化合价一定大于X元素 | |
| B. | 三种元素原子半径由高到低的顺序一定是Y>X>Z | |
| C. | 若它们的原子最外层电子数之和为11,则X为金属元素 | |
| D. | 若它们均为金属元素,则Y的最高价氧化物对应水化物的碱性最强 |
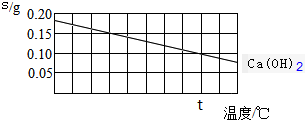
| A. | 氢氧化钙的溶解是吸热过程 | |
| B. | 温度升高时氢氧化钙溶解的速度减慢 | |
| C. | t℃时氢氧化钙的Ksp约等于2.46×10-4 | |
| D. | 向含有Ca(OH)2和Mg(OH)2两种沉淀的悬浊液中滴加NaOH浓溶液,分散系中$\frac{c(C{a}^{2+})}{c(M{g}^{2+})}$的比值不变 |
 乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)
乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(1)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-;HC2O4-?H++C2O42-,.
(2)KHC2O4溶液显酸性的原因是HC2O4-的电离程度大于水解程度;向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-)
b.c(Na+)=c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-)
d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O;又知该反应开始时速率较慢,随后大大加快,可能的原因是反应生成的Mn2+对该反应具有催化作用.
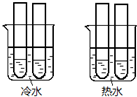
(4)某同学设计实验如图所示:两个烧杯中的试管都分别盛有2mL 0.1 mol/L H2C2O4溶液和4mL 0.1mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对反应速率的影响,但该实验始终没有看到溶液褪色,推测原因KMnO4溶液过量.
(5)已知草酸(H2C2O4)受热分解的化学方程式为:H2C2O4→H2O+CO↑+CO2↑,写出FeC2O4在密闭容器中高温分解的化学方程式FeC2O4$\frac{\underline{\;高温\;}}{\;}$Fe+2CO2↑.
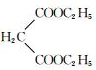 $→_{CH_{3}CH_{2}ONa}^{BrCH_{2}CH_{2}CH_{2}Br}$
$→_{CH_{3}CH_{2}ONa}^{BrCH_{2}CH_{2}CH_{2}Br}$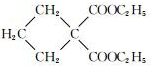 $→_{ii.H+/△}^{i.H_{2}O,OH-}$
$→_{ii.H+/△}^{i.H_{2}O,OH-}$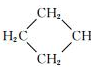 -COOH
-COOH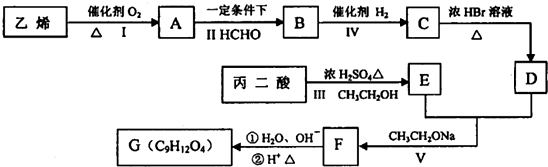
 G
G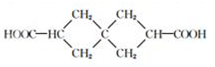
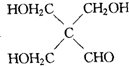
 例如:
例如: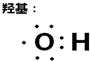
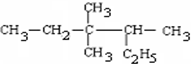 的名称3,3,4-三甲基己烷
的名称3,3,4-三甲基己烷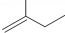 的名称2-甲基-1-丁烯.
的名称2-甲基-1-丁烯.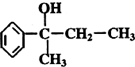 在工业上用基础的石油产品(乙烯、丙烯等)进行合成.合成A的过程可表示为:
在工业上用基础的石油产品(乙烯、丙烯等)进行合成.合成A的过程可表示为: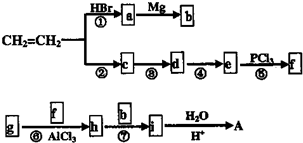
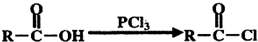
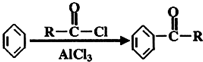
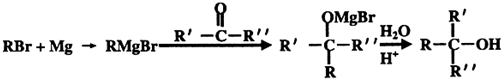
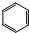 ;
;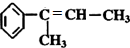 .
.