题目内容
5.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 能使甲基橙变红的溶液中:Na+、Fe2+、SO42-、MnO4- | |
| B. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:K+、Na+、Cl-、HCO3- | |
| C. | 0.1 mol•L-1的NH4I溶液中:Mg2+、Na+、ClO-、NO3- | |
| D. | 0.1 mol•L-1的CuSO4溶液中:Mg2+、Al3+、Br-、Cl- |
分析 A.使甲基橙变红的溶液为酸性溶液,高锰酸根离子在酸性条件下能够氧化亚铁离子;
B.该溶液为碱性溶液,溶液中存在大量氢氧根离子,碳酸氢根离子与氢氧根离子反应;
C.镁离子与次氯酸根离子发生双水解反应,次氯酸根离子能够氧化碘化铵电离出的碘离子;
D.四种离子之间不反应,都不与硫酸铜溶液反应.
解答 解:A.使甲基橙变红的溶液中存在大量氢离子,酸性条件下Fe2+、MnO4-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.该溶液为碱性溶液,HCO3-与碱性溶液中的氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.Mg2+、ClO-之间发生双水解反应,ClO-且能够氧化NH4I电离出的I-,在溶液中不能大量共存,故C错误;
D.Mg2+、Al3+、Br-、Cl-之间不不发生反应,都不与CuSO4溶液反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
15.下列观点中不正确的是( )
| A. | 通过化学变化一定能改变物质的性质 | |
| B. | 人们所使用的材料,都是纯度越高越好 | |
| C. | 氧化还原反应中一定会发生电子转移 | |
| D. | 某元素由化合态变为游离态,该元素有可能被氧化,也有可能被还原 |
16.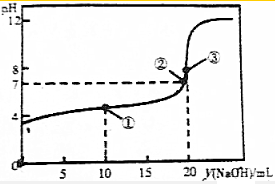 常温下,在20mL0.1mol•L-1 H2R溶液中滴加0.1mol•L-1 NaOH溶液,混合溶液的pH与滴加氢氧化钠溶液体积(V)的关系如图所示.下列说法不正确的是( )
常温下,在20mL0.1mol•L-1 H2R溶液中滴加0.1mol•L-1 NaOH溶液,混合溶液的pH与滴加氢氧化钠溶液体积(V)的关系如图所示.下列说法不正确的是( )
 常温下,在20mL0.1mol•L-1 H2R溶液中滴加0.1mol•L-1 NaOH溶液,混合溶液的pH与滴加氢氧化钠溶液体积(V)的关系如图所示.下列说法不正确的是( )
常温下,在20mL0.1mol•L-1 H2R溶液中滴加0.1mol•L-1 NaOH溶液,混合溶液的pH与滴加氢氧化钠溶液体积(V)的关系如图所示.下列说法不正确的是( )| A. | HR-的电离程度大于水解程度 | |
| B. | ②点对应溶液中离子浓度的关系c(Na+)<c(H2R)+c(HR-)+c(R2-) | |
| C. | 在①、②、③点对应的溶液中,水电离的c(H+)•c(OH-)最大的是③ | |
| D. | 滴定前,溶液中存在粒子浓度大小关系:c(H2R)>c(H+)>c(HR-)>c(R2-)>c(OH-) |
10.已知:①2H2O(l)═2H2(g)+O2(g)△H1
②H2(g)+Cl2(g)═2HCl(g)△H2
③4HCl(g)+O2(g)═2Cl2(g)+2H2O(g)△H3
④N2(g)+3H2(g)?2NH3(g)△H4
⑤2NH3(g)+3Cl2(g)═N2(g)+6HCl(g)△H5
下列关于上述反应焓变的判断正确的是( )
②H2(g)+Cl2(g)═2HCl(g)△H2
③4HCl(g)+O2(g)═2Cl2(g)+2H2O(g)△H3
④N2(g)+3H2(g)?2NH3(g)△H4
⑤2NH3(g)+3Cl2(g)═N2(g)+6HCl(g)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0,△H2>0 | B. | △H3>0,△H4>0 | C. | 3△H2=△H4+△H5 | D. | △H3=-(△H1+2△H2) |
14.在下列酸性溶液中,因发生氧化还原反应而不能大量共存的是( )
| A. | Ag+、NO3-、Cl-、K+ | B. | Cu2+、NH4+、Br-、OH- | ||
| C. | Ag+、Ba2+、OH-、SO42- | D. | Fe2+、Na+、NO3-、SO42- |
15.下列物质间的转化不能通过一步转化实现的是( )
| A. | Na2CO3→Na0H | B. | Fe→Cu | C. | Cu→Cu(OH)2 | D. | CaCl2→CaCO3 |
 (NH4)2SO4•MnSO4•nH2O(硫酸锰铵)是浅粉色晶体,易溶于水,在农业上用作微量元素肥料,实验室由MnO2制备硫酸锰铵的实验步骤如下:
(NH4)2SO4•MnSO4•nH2O(硫酸锰铵)是浅粉色晶体,易溶于水,在农业上用作微量元素肥料,实验室由MnO2制备硫酸锰铵的实验步骤如下: