题目内容
12.下列化合物中,既含有离子键、又含有共价键的是( )| A. | HCl | B. | Na2O2 | C. | H2O | D. | CaCl2 |
分析 一般来说,活泼金属元素与活泼非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A、HCl只含共价键,故A错误;
B、Na2O2中钠离子与过氧根离子间形成离子键,O与O间形成非极性共价键,故B正确;
C、H2O中只含有共价键,故C错误;
D、CaCl2中只含有离子键,故D错误;
故选B.
点评 本题考查化学键,把握化学键形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
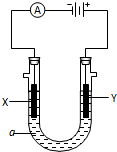
7. 如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )
如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )
 如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )
如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )| A. | 向A池中通入4.48 L HCl气体可恢复到电解前的状态 | |
| B. | 停止通电后恢复至室温A池中溶液的pH值为14 | |
| C. | 电极e应为粗铜板材料且质量减少6.4 g | |
| D. | 该电路中通过的电子的物质的量为0.4 mol |
17.下列叙述正确的是( )
| A. | 1个甘氨酸分子中存在9对共用电子对(甘氨酸的结构简式为NH2-CH2-COOH) | |
| B. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 | |
| C. | H2S和CS2分子都是含极性键的极性分子 | |
| D. | 熔点由高到低的顺序是:金刚石>碳化硅>晶体硅 |
1.下列各分子中所有原子都满足最外层为8电子结构的是( )
| A. | BeCl2 | B. | HCl | C. | PCl5 | D. | CO2 |
2.下列气体不会造成大气污染的是( )
| A. | 二氧化硫 | B. | 氮气 | ||
| C. | 一氧化碳 | D. | 一氧化氮和硫酸铵 |
 ;③C、D形成的化合物的电子式
;③C、D形成的化合物的电子式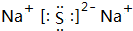 ;
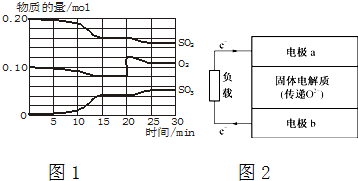
;
 某化学实验小组需要2mol•L-1的NaCl溶液98ml,现用NaCl固体来配制,请回答下列问题:
某化学实验小组需要2mol•L-1的NaCl溶液98ml,现用NaCl固体来配制,请回答下列问题: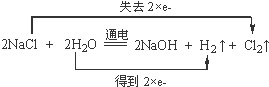 ;
;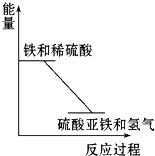 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示: